Syrer og baser er to kemiske grupper relateret til hinanden. De er to stoffer af stor betydning og findes i hverdagen.
Syrer og baser undersøges af uorganisk kemi, den gren, der studerer forbindelser, der ikke er dannet af kulstof.
Syrer og baser Begreber
Begrebet Arrhenius
Et af de første koncepter for syrer og baser udviklet i slutningen af det 19. århundrede af Svante Arrhenius, en svensk kemiker.
Ifølge Arrhenius er syrer stoffer, der i vandig opløsning lider ionisering, frigiver kun som kationer H +.
HCI (aq) → H+ (aq) + Cl- (her)
I mellemtiden er baser stoffer, der lider ionisk dissociationfrigivelse af OH- (hydroxyl) ioner som den eneste type anion.
NaOH (aq) → Na+ (aq) + OH- (her)
Arrhenius 'koncept for syrer og baser viste sig imidlertid at være begrænset til vand.
Læs også om: Arrhenius teori og Neutraliseringsreaktion.
Bronsted-Lowry-konceptet
Bronsted-Lowry-konceptet er bredere end Arrhenius og blev introduceret i 1923.
Ifølge denne nye definition er syrer stoffer, der er i stand til at donere en proton H
+ til andre stoffer. Og baser er stoffer, der er i stand til at acceptere en H-proton+ af andre stoffer.Det vil sige syre er en protondonor, og basen er en protonreceptor.
Det karakteriserer en stærk syre som en, der fuldstændigt ioniserer i vand, dvs. frigiver H-ioner+.
Stoffet kan imidlertid være amfiprotisk, dvs. i stand til at opføre sig som en syre eller Bronsted base. Se på eksemplet med vand (H2O), et amfiprotisk stof:
HNO3(aq) + H2O(l) → NEJ3- (aq) + H3O+(aq) = Bronsted base, accepterede protonen
NH3(aq) + H2O(l) → NH4+(aq) + OH-(aq) = Bronsted syre, doneret protonen
Desuden opfører stoffer sig som konjugerede par. Alle reaktioner mellem en syre og en grundlag af Bronsted involverer overførsel af en proton og har to konjugerede syre-basepar. Se eksemplet:
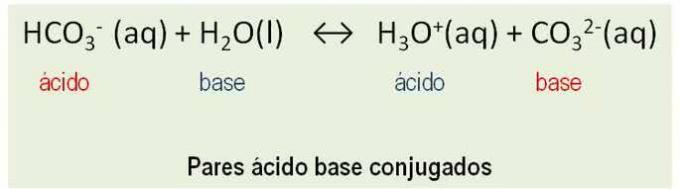
HCO3- og CO32-; H2O og H3O+ er konjugatsyrebasepar.
Lær mere om:
- Uorganiske funktioner
- Syre-base indikatorer
- Titrering
Syrenomenklatur
For at definere nomenklaturen opdeles syrer i to grupper:
- Hidracids: syrer uden ilt;
- Oxysyrer: syrer med ilt.
Hidracids
Nomenklaturen forekommer som følger:
syre + elementnavn + hydric
Eksempler:
HCI = saltsyre
HI = hydriodinsyre
HF = flussyre
oxysyrer
Nomenklaturen for oxysyrer følger følgende regler:
Du standard syrer af hver familie (familierne 14, 15, 16 og 17 i det periodiske system) følger den generelle regel:
syre + elementnavn + ic
Eksempler:
HC13 = klorsyre
H2KUN4 = svovlsyre
H2CO3: kulsyre
For de andre syrer, der dannes med det samme kerneelement, navngiver vi dem baseret på mængden af ilt efter følgende regel:
| Mængde ilt i forhold til standardsyre | Nomenklatur |
|---|---|
| + 1 ilt | Syre + pr. + Elementnavn + ico |
| - 1 ilt | Syre + elementnavn + knogle |
| - 2 oxygener | Syre + hypo + elementnavn + knogle |
Eksempler:
HC14 (4 oxygenatomer, et mere end standardsyre): perchlorsyre;
HC12 (2 iltatomer, et mindre end standardsyre): klorsyre;
HClO (1 iltatom, to mindre end standard syre): hypochlorsyre.
Du kan også være interesseret i: svovlsyre
Basisnomenklatur
For basisnomenklatur følges den generelle regel:
Hydroxid + kationnavn
Eksempel:
NaOH = Natriumhydroxid
Men når det samme element danner kationer med forskellige ladninger, tilføjes ionens ladning til slutningen af navnet i romertal.
Eller du kan tilføje suffikset -oso til den mindst ladede ion og suffikset -ico til den mest ladede ion.
Eksempel:
Jern
Tro2+ = Fe (OH)2 = Jern II-hydroxid eller jernholdigt hydroxid;
Tro3+ = Fe (OH)3 = Jern III-hydroxid eller jernhydroxid.
Sørg for at tjekke indgangsspørgsmål om emnet med kommenteret opløsning i: Øvelser på uorganiske funktioner.