De periodiske egenskaber ved kemiske grundstoffer er de egenskaber, de har.
Bemærk, at de kemiske grundstoffer i det periodiske system har en bestemt placering, der varierer alt efter de periodiske egenskaber, de udviser. De er sorteret i stigende atomnummerrækkefølge.
I henhold til Moseleys lov:
“Mange fysiske og kemiske egenskaber af grundstoffer varierer periodisk i rækkefølgen af grundstoffernes atomnummer..”
Vigtigste periodiske egenskaber
atomær radius
Relateret til størrelsen på atomer er denne egenskab defineret af afstanden mellem kernerne i kernerne af to atomer af det samme element.
Derfor er den atomstråle svarer til halvdelen af afstanden mellem kernerne i to nærliggende atomer, udtrykt som følger:
r = d / 2
Hvor:
r: lyn
d: internuklear afstand
Det måles i picometre (om eftermiddagen). Denne måling er en delmultipel af måleren:
13.00 = 10-12 m
I det periodiske system stiger atomradius fra top til bund i lodret position. På vandret stiger de fra højre til venstre.
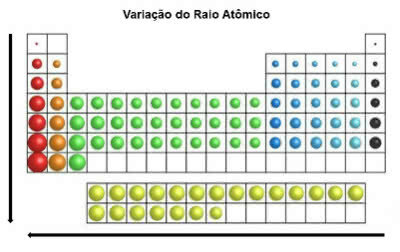
Atomic Radius Variation
Det kemiske element, der har den største atomare radius, er cæsium (Cs).
Atomisk volumen
Denne periodiske egenskab angiver volumenet optaget af 1 mol af elementet i fast tilstand.
Det er værd at bemærke, at atomvolumenet ikke er volumenet på 1 atom, men et sæt på 6,02. 1023 atomer (1 mol værdi)
Atommets atomvolumen defineres ikke kun af volumenet af hvert atom, men også afstanden mellem disse atomer.
I det periodiske system stiger atomvolumenværdierne fra top til bund (lodret) og fra centrum til kant (vandret).

Atomisk volumenvariation
For at beregne atomvolumenet anvendes følgende formel:
V = m / d
Hvor:
V: atomvolumen
m: masse på 6,02. 1023 elementatomer
d: solid state element tæthed
Absolut tæthed
DET massefylde absolut, også kaldet "specifik masse", er en periodisk egenskab, der bestemmer forholdet mellem massen (m) af et stof og volumenet (v) optaget af massen.
Det beregnes ved hjælp af følgende formel:
d = m / v
Hvor:
d: massefylde
m: pasta
v: volumen
I det periodiske system stiger densitetsværdier fra top til bund (lodret) og fra kanter til center (vandret).
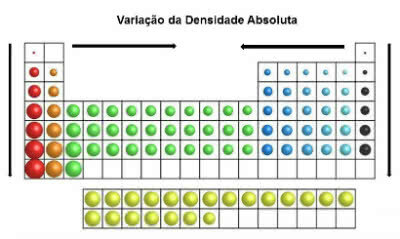
Absolut tæthedsvariation
Således er de tætteste elementer i midten og nederst på bordet:
Osmium (Os): d = 22,5 g / cm3
Iridium (Ir): d = 22,4 g / cm33
Smeltepunkt og kogepunkt
En anden vigtig periodisk egenskab er relateret til de temperaturer, som elementerne indgår i smelter og koger.
Smeltepunktet (MP) er temperaturen, ved hvilken stof passerer fra den faste fase til den flydende fase. Kogepunktet (PE) er den temperatur, hvor materialet passerer fra væsken til den gasformige fase.
I det periodiske system varierer værdierne for PF og PE alt efter de sider, der er placeret i tabellen.
Lodret og på venstre side af bordet stiger de fra bunden til toppen. På højre side øges de fra top til bund. I vandret retning strækker de sig fra enderne til midten.

Smelte- og kogepunktsvariation
Elektronisk affinitet
Også kaldet “elektroaffinitet”, det er den mindste energi, der kræves af et kemisk element for at fjerne en elektron fra en anion.
Det vil sige elektronisk affinitet angiver mængden af frigivet energi, når et elektron modtages af et atom.
Bemærk, at dette ustabile atom er alene og i gasform. Med denne egenskab opnår den stabilitet, når den modtager elektronen.
I modsætning til atomradius vokser elementernes elektroaffinitet i det periodiske system fra venstre til højre, vandret. I lodret retning stiger den fra bunden til toppen.
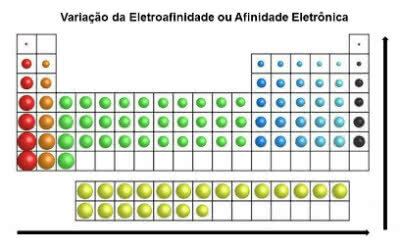
Elektronisk affinitetsvariation
Det kemiske element, der har den største elektronaffinitet, er klor (Cl) med en værdi på 349 KJ / mol.
Ioniseringsenergi
Også kaldet "ioniseringspotentiale”, Denne egenskab er i modstrid med den elektroniske tilknytning.
Det er den mindste energi, der kræves af et kemisk element for at fjerne en elektron fra et neutralt atom.
Således angiver denne periodiske egenskab, hvor meget energi der er brug for til at overføre elektronen fra et atom i jordtilstand.
Den såkaldte "grundtilstand for et atom" betyder, at dets antal protoner er lig med antallet af elektroner (p+ = og-).
Efter at have fjernet en elektron fra atomet ioniseres den således. Det vil sige, det får flere protoner end elektroner og bliver derfor en kation.
I det periodiske system er ioniseringsenergien i strid med atomradiusens. Så det stiger fra venstre mod højre og fra bund til top.
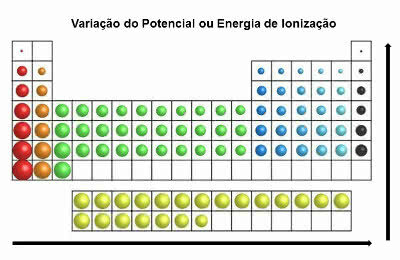
Ionisering Energivariation
De grundstoffer, der har det største ioniseringspotentiale, er fluor (F) og klor (Cl).
elektronegativitet
Egenskaber for atomer af grundstoffer, der har en tendens til at modtage elektroner i en kemisk binding.
Det forekommer i kovalente bindinger på tidspunktet for deling af elektronpar. Når man modtager elektroner, er atomer tilbage med en negativ ladning (anion).
Husk at dette betragtes som den vigtigste egenskab ved det periodiske system. Dette skyldes, at elektronegativitet inducerer atomenes opførsel, hvorfra molekyler dannes.
I det periodiske system elektronegativitet stiger fra venstre mod højre (vandret) og fra bund til top (lodret)
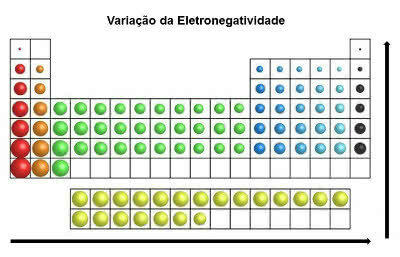
Elektronegativitetsvariation
Således er det mest elektronegative element i det periodiske system fluor (F). På den anden side er Cæsium (Cs) og Francium (Fr) de mindst elektronegative elementer.
elektropositivitet
I modsætning til elektronegativitet indikerer denne egenskab ved elementære atomer tendenser til at miste (eller opgive) elektroner i en kemisk binding.
Når man mister elektroner, får elementernes atomer en positiv ladning og danner således en kation.
I samme retning som atomradiusen og i modsætning til elektronegativitet, i det periodiske system a elektropositivitet stiger fra højre til venstre (vandret) og fra top til bund (lodret).
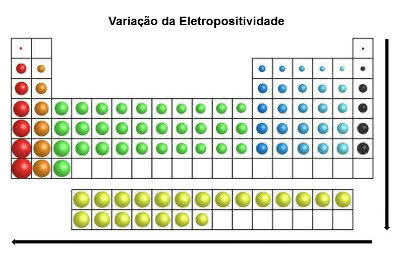
Elektropositivitetsvariation
De kemiske grundstoffer med den højeste elektropositivitet er metaller, og af denne grund kaldes denne egenskab også "metallisk karakter". Det mest elektropositive element er Francium (Fr) med maksimal tendens til oxidation.
Opmærksomhed!
Dig "ædle gasser”Er inerte elementer, da de ikke udfører kemiske bindinger og næppe donerer eller modtager elektroner. De har også vanskeligheder med at reagere med andre elementer.
Derfor overvejes ikke disse elementers elektronegativitet og elektropositivitet.
Læs også:
- Kemiske bindinger
- Det periodiske systems historie
- Periodiske bordfamilier
Aperiodiske egenskaber
Ud over periodiske egenskaber har vi aperiodiske egenskaber. I dette tilfælde øges eller formindskes værdierne med det atomare antal grundstoffer.
De modtager dette navn, da de ikke adlyder deres position på det periodiske system som periodiske. Det vil sige, de gentages ikke på regelmæssige tidspunkter.
De vigtigste aperiodiske egenskaber er:
- Atommasse: Denne egenskab stiger, når atomnummeret stiger.
- Specifik varme: denne egenskab falder med stigende atomnummer. Husk, at specifik varme er den mængde varme, der er nødvendig for at øge temperaturen med 1 ° C på 1 g af elementet.
Entréeksamen Øvelser med feedback
1. (PUC-RJ) Overvej udsagnene om gruppe IA-elementer i det periodiske system
JEG. De kaldes alkalimetaller.
II. Dens atomstråler vokser med atomnummeret.
III. Dets ioniseringspotentiale stiger med atomnummer.
IV: Dens metalliske karakter stiger med atomnummer.
Blandt udsagnene er sande:
a) I og II
b) III og IV
c) I, II og IV
d) II, III og IV
e) I, II, III og IV
Alternativ c
2. (UFMG) Sammenligning af klor og natrium, de to kemiske grundstoffer, der danner bordsalt, kan du sige, at klor:
a) er tættere.
b) er mindre flygtig.
c) har en større metallisk karakter.
d) har lavere ioniseringsenergi.
e) har en mindre atomradius.
Alternativ og
3. (UFC-CE) Den fotoelektriske effekt består af emission af elektroner fra metalliske overflader gennem forekomsten af lys med passende frekvens. Dette fænomen er direkte påvirket af ioniseringspotentialet for metaller, som stort set har været anvendes til fremstilling af fotoelektroniske enheder, såsom: fotoceller til offentlig belysning, kameraer fotografisk osv. Baseret på variationen i elementernes ioniseringspotentiale i det periodiske system, skal du markere det alternativ, der indeholder det metal, der mest sandsynligt viser den fotoelektriske effekt.
a) Fe
b) Hg
c) Cs
d) Mg
e) Ca
Alternativ c
Tjek spørgsmål til optagelseseksamen med en kommenteret opløsning i Øvelser på det periodiske system og upublicerede spørgsmål om emnet i Øvelser i organisering af det periodiske system.
Læs også:
- Periodiske system
- Elektronisk distribution
- Kemiske grundstoffer
- Intermolekylære kræfter