DET aktiveringsenergi det er den mindste mængde energi, der er nødvendig for, at kollisionen mellem reaktantpartiklerne, lavet i en gunstig orientering, finder sted og resulterer i en reaktion.
Reaktioner forekommer kun, når reaktanterne har aktiveringsenergi (eller den nødvendige minimale energi, der varierer fra reaktion til reaktion; enten i mængde eller form) eller når den leveres til dem.
For eksempel, når metallisk natrium kommer i kontakt med vand, reagerer det voldsomt. Dette betyder, at energiindholdet i disse reaktanter allerede er tilstrækkeligt til, at reaktionen finder sted.
I tilfælde af tænding af en ovn vil forbrændingsreaktionen kun forekomme, hvis vi placerer en tændstik eller en anden ildkilde i nærheden af den gas, der frigøres af ovnen. Dette betyder, at det i dette tilfælde var nødvendigt at levere energi til systemet, så det nåede aktiveringsenergien, og reaktionen fandt sted.
I tilfældet med den anvendte fosfor tilvejebringes aktiveringsenergien ved friktion, så den kan forbrændes. Det samme sker med lightere, som også har brug for en gnist, der giver den nødvendige aktiveringsenergi til forbrænding af gassen indeholdt i dem.
Aktiveringsenergi kan også tilvejebringes af lys, som det er tilfældet med nedbrydning af hydrogenperoxid. Derfor opbevares den i mørke eller uigennemsigtige flasker.
Stop ikke nu... Der er mere efter reklamen;)

Således kan vi konkludere, at aktiveringsenergien (E.så længe) er forskellen mellem den nødvendige energi til reaktionens start (E) og energien indeholdt i reaktanterne (E.pr):

Aktiveringsenergi er en hindring for, at reaktionen kan finde sted, og det er nødvendigt at bryde bindingerne af reaktanter. Med dette finder reaktionen sted, og der oprettes nye forbindelser for at danne produkterne.
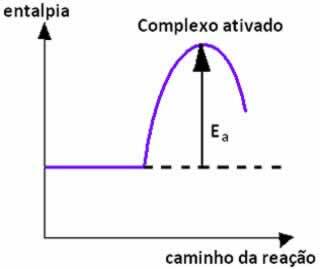
Når kollisionen mellem partikler af reaktanter med gunstig orientering sker med samme energi eller højere end aktiveringsenergien, inden dannelsen af produkterne dannes en mellemliggende og ustabil tilstand, denomineret kompleks aktiveret, hvor reaktantbindingerne svækkes, og produktbindingerne dannes. Dermed, aktiveringsenergi er den nødvendige energi til dannelse af det aktiverede kompleks.
Nedenfor har vi en graf, der viser aktiveringsenergien som en barriere for reaktionen at finde sted:
Af Jennifer Fogaça
Uddannet i kemi
Vil du henvise til denne tekst i et skole- eller akademisk arbejde? Se:
FOGAÇA, Jennifer Rocha Vargas. "Aktiveringsenergi"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/energia-ativacao.htm. Adgang til 27. juni 2021.