Overvej følgende kemiske ligevægt ved en konstant temperatur:
3 timer2 (g) + N2 (g) NH 2 NH3 (g)
Ifølge Gay-Lussac er andelen af volumener af gasformige deltagere i en reaktion lig med forholdet mellem de respektive støkiometriske koefficienter. Enkelt sagt kan vi sige, at antallet af molekyler, der er til stede i reaktanterne og produkterne, er lig med koefficienterne i ligningen.
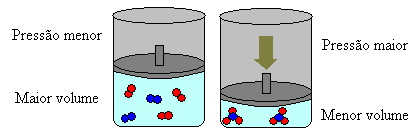
I ovenstående tilfælde har vi i reagenserne 4 molekyler, og i produkterne har vi 2 molekyler, hvilket betyder, at volumenet af reagenserne er større, og produktets volumen er mindre.
Hvis vi øger trykket i dette system, skifter balancen mod det mindre volumen for at mindske dette tryk. I tilfælde af den reaktion, vi overvejer, vil forskydningen være i direkte retning af produktdannelse (NH3 (g)).
Men hvis vi sænker trykket, vil reaktionen bevæge sig mod det største volumen, som er den modsatte retning, af dannelse af reaktanter (3H2 (g) + N2 (g)).
Stop ikke nu... Der er mere efter reklamen;)
Dette sker i henhold til Le Chateliers princip, der siger, at enhver forstyrrelse (såsom nedsættelse eller forøgelse af trykket) forårsagede i et system i ligevægt får det til at bevæge sig i den retning, der minimerer denne forstyrrelse, og omjusterer sig til en ny balance.
Kort kan vi sige følgende i tilfælde af indflydelse af trykvariation på kemisk ligevægt:
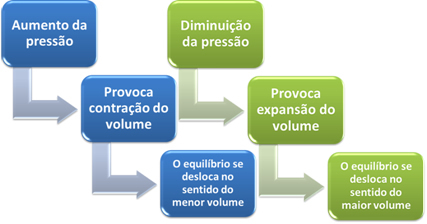
I tilfælde af reaktioner, hvor volumenet af reaktanterne er lig med volumenet af produkterne, ændres den kemiske ligevægt ikke.
Af Jennifer Fogaça
Uddannet i kemi
Vil du henvise til denne tekst i et skole- eller akademisk arbejde? Se:
FOGAÇA, Jennifer Rocha Vargas. "Variation af tryk og forskydning af kemisk balance"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/variacao-pressao-deslocamento-equilibrio-quimico.htm. Adgang til 28. juni 2021.
Kemi

Test din viden og lær mere med denne liste over løste øvelser på kemiske balancer. Gennem dette materiale vil du være i stand til bedre at forstå, hvordan man arbejder med ligevægtskonstanter (Kp, Kc og Ki), ligevægtsforskydning, pH og pOH samt ligevægt i såkaldte bufferopløsninger.