Den organiske gruppe alkoholer er velkendt inden for organisk kemi og er kendetegnet ved tilstedeværelsen af en hydroxyl (OH) bundet til et mættet carbon. Der er alkoholer, der er umættede, som but-3-en-1-ol nedenfor:
H2C ═ CH ─ CH2 CH2 ─ åh
Imidlertid har nogle forbindelser hydroxyl direkte bundet til et carbon med en dobbeltbinding. Denne type forbindelse er ikke en alkohol, den hører til den organiske funktion kaldet: enol.
Enoler er derfor karakteriseret ved følgende funktionelle gruppe:
│
─ C ═ CH ─ åh
Nomenklaturen for enoler er lavet i henhold til følgende skema:
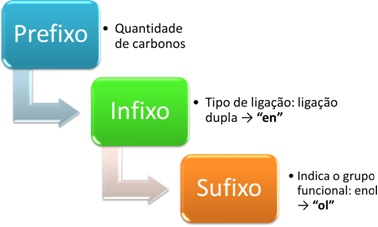
Overvej f.eks. Følgende enklere enol:
H2C CH ─ åh
Præfiks: har 2 carbonatomer: et
Infix: dobbeltbinding: da → ethylen
Suffiks: enol: Hej
I tilfælde af ethenol var det ikke nødvendigt at nummerere placeringen af den funktionelle gruppe eller umættethed, fordi der ikke var nogen anden mulighed. Men i nedenstående tilfælde er det nødvendigt:
H3C - CH═CH - OH: prop-1-en-1-ol
H3C - C═CH2: prop-1-en-2-ol
│
Åh
H3C - CH═C CH2 CH3: pent-2-en-3-ol
│
Åh
H3C - C═CH CH3: men-2-en-2-ol
│
Åh
Enoler er meget ustabile forbindelser, da de kan gennemgå en type dynamisk isomerisme kaldet tautomery, hvor isomerer eksisterer sammen i dynamisk ligevægt i den samme flydende fase.
Stop ikke nu... Der er mere efter reklamen;)
Ilten i enol er meget elektronegativ, hvilket tiltrækker elektronerne fra dobbeltbindingen af kulstof, som er en svag binding, der er let at fortrænge, og danner et aldehyd eller en keton.
For eksempel omdannes en lille del i en eddikesyde-aldehydopløsning (ethanal) til ethenol, som igen regenereres tilbage til aldehyd. Der er således en kemisk balance mellem disse forbindelser, der har den samme molekylformel C2H4O:
Ethanal Ethanol
Åh
║ │
H3Ç - Ç - H ↔ H2Ç ═ C - H
enolaldehyd
En anden enol, prop-1-en-2-ol, kan gå i dynamisk ligevægt med en keton, propanon:
Propanon Prop-1-en-2-ol
OH OH
║ │ │
H3C - C - C - H ↔ H2Ç ═ C - CH2
enolketon
For flere detaljer, læs teksten: Dynamisk forfatningsmæssig isomerisme eller tautomery.
Af Jennifer Fogaça
Uddannet i kemi
Vil du henvise til denne tekst i et skole- eller akademisk arbejde? Se:
FOGAÇA, Jennifer Rocha Vargas. "Enols og dets nomenklatur"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/enois-sua-nomenclatura.htm. Adgang til 27. juni 2021.
Kemi

Gå ind på dette link og lær om den organiske funktion af phenoler, en gruppe iltede stoffer, fra stor reaktivitet, hvis surhed er større end alkoholerne (forbindelser, der også har en gruppe hydroxyl). Dens struktur skiller sig ud ved præsentation af en hydroxidgruppe (OH) direkte bundet til en aromatisk forbindelse.
Hovedfenoler, aspirin, pikrinsyre, bakelitter, phenolphthaleinafvisende egenskab cresol, creolin, lysol, cresols, olie taget fra kultjære, fremstilling af konserveringsmidler til træ.
Kemi
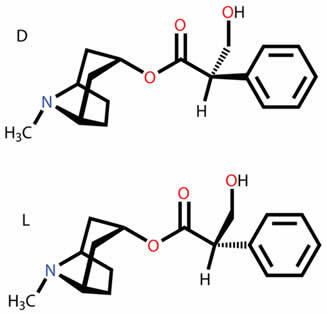
Ved hvad de forskellige typer plane og rumlige isomerer handler om, såsom funktion, position, kæde, tautomerisme, metamerisme, cis-trans geometrisk og optisk isomerisme.
Kemi

Hydroxylfunktionel gruppe, Primære alkoholer, Sekundære alkoholer, Tertiære alkoholer, Methanol, Glycerol, Ethanol, fremstilling af nitroglycerin, fremstilling af maling, produktion af alkoholholdige drikkevarer, eddikesyre, brændstof biler.


