Text Reakce sčítání ukázal, že tyto typy organických reakcí jsou pojmenovány tímto způsobem, protože reaktant je přidáván do organické molekuly rozbitím vazeb mezi uhlíky. V tomto textu byl ukázán případ alkenů, zde již budeme uvažovat o tom, jak k tomu dochází u alkynů, nebo to znamená s těmi uhlovodíky (složenými pouze z atomů uhlíku a vodíku), které mají vazbu trojnásobný.
Zranitelným bodem alkynů je přesně trojná vazba, kde mohou být rozbity vazby typu pi (π) (přidání částečné) nebo dvakrát (úplné přidání) a vzniknou nové sloučeniny s dvojnými (alkeny) nebo jednoduchými vazbami (alkany).
Podívejme se na případy adičních reakcí v alkynech:
1. Přidání vodíku nebo hydrogenace:
V tomto případě molekula H2 se k alkinu přidává za použití katalyzátoru, kterým je obvykle práškový nikl (Ni), platina (Pt) nebo palladium (Pd). Vzhledem k potřebě použít katalyzátor se tato reakce také nazývá katalytická hydrogenace a vyskytuje se to ve fázích: v první fázi dostanete alken a ve druhé fázi, která je pomalejší, dostanete alkan.
Pokud je použitý katalyzátor silný, jako je nikl a platina, reakce přímo produkuje alkan. Palladium smíchané s BaSO4 je slabým katalyzátorem a produkuje alken. Je také možné použít částečný inhibitor katalyzátoru k dosažení pouze po alken. Tato reakce také probíhá za vysokých tlaků a teplot.
Dále přidáme vodík do etanu, čímž vznikne ethylen a poté etan:

2. Přidání halogenů nebo halogenace:
Alkynová pí vazba je přerušena a do molekuly jsou přidány dva atomy halogenu (prvky z rodiny 17A periodické tabulky, nejpoužívanější jsou: Cl2 a Br2), tvořící vicinální dihalogenid, což znamená, že dva atomy halogenu jsou vázány na sousední atomy uhlíku. Reakce může pokračovat, rozbít druhou pí vazbu a přidat k molekule další dva atomy halogenu.
V níže uvedeném příkladu máme tento typ příplatku k úplatku:
ClCl ClCl
││ ││
H ─C ≡ C CH3 + Cl2 → H ─ C ═ C CH3 + Cl2 → H ─ C ─ C CH3
││
ClCl
ALCINO DI-HALETOVÁ TETRAHALETA
3. Přidání halogenovodíku (halogenhydridy nebo hydrohalogenace):
Zde se k alkinu přidá halogenovodík a může také dojít k částečnému a úplnému přidání. Důležitým aspektem tohoto typu reakce je, že následuje Markovnikovovo pravidlo, to znamená, že vodík se váže na více hydrogenovaný uhlík (s připojeným více atomy vodíku) a halogen se váže na méně hydrogenovaný uhlík.
Při totální hydrohalogenaci vzniká gemický dihalogenid, tj. Sloučenina, která má dva atomy halogenu připojené ke stejnému uhlíku.
Nepřestávejte... Po reklamě je toho víc;)
Hodinky:
HBr Hbr
││ ││
H ─C ≡ C CH3 + HBr → H ─ C ═ C CH3 + HBr → H ─ C ─ C CH3
││
Hbr
ALCINO HALIDOVÝ GEMOVÝ DI-HALOGID
Důležitým příkladem tohoto typu reakce je reakce, ke které dochází při přidání chlorovodíku k ethynu za vzniku chlorethen nebo vinyl monochlorid, což je monomer, který tvoří polymer polyvinylchloridu, lépe známý pod zkratkou PVC.
HClHCl
││ ││
H ─C ≡ C ─ H + HCl → H ─ C ═ C ─ H + HCl → H ─ C ─ C ─ H
││
HCl
ETHINO CHLOROETEN 1,1-DICHLOROETHAN
(PVC monomer)
PVC je látka široce používaná v průmyslu pro výrobu různých produktů, jako jsou sandály, lékovky, zdravotnické prostředky, plastové kalhotky pro kojence, tašky, potahy drátů, hračky, čalounění nábytku, čalounění automobilů, pláštěnky, plastové boty, vinylové desky, podlahy, balicí fólie, trubky používané ve vodních potrubích a kanalizace atd.
4. Přidání vody (hydratace):
Při této reakci voda reaguje s alkynem a zpočátku vytváří enol, který prochází molekulárním přesmykem a mění se na aldehyd (v případě alkynů menších než acetylen). Enol a aldehyd zůstávají v dynamické rovnováze s převahou aldehydu. Toto je případ Dynamic Constitucikonal Isomery or Tautomery.
Příklad:

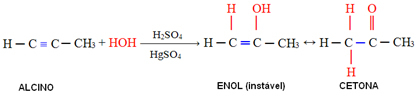
V případě alkynů větších než acetylen se postupuje podle Markovnikovova pravidla a z enolu vzniká keton:
Autor: Jennifer Fogaça
Vystudoval chemii