definice hmota je dáno jednoduchou a komplexní frází: je to všechno, co zaujímá místo (stejné jako objem) v prostoru a má váhu (součin hmotnosti a gravitace). Některé příklady hmoty: strom, bakterie, virus, člověk, vzduch, voda, stůl, vozidlo atd.
Mohli bychom uvést tisíce příkladů hmota je to docela komplexní. Existuje ale něco, na čem nezáleží? Samozřejmě ano, v tomto případě se to však nazývá energie, jako v následujících příkladech:
Světlo: nazývaná světelná energie;
Tlak: nazývaná tlaková energie;
Zvuk: zvaná zvuková energie;
Oheň: sdružení tepelné a světelné energie;
Elektřina: zvaná elektrická energie;
Teplo: nazývaná tepelná energie;
Rentgen: forma elektromagnetické energie;
THE energie lze definovat jako a síla schopné vyvolat akci a pohyb. Je tedy velmi jednoduché odlišit hmotu od energie, protože jeden zabírá prostor a má hmotu a druhý nikoli.
Důležitá kuriozita o hmota je, že jej lze volat dvěma různými způsoby: tělo a objekt.
Tělo: je součástí hmota. Příklady: vlněná příze, rozbité sklo, vítr, kmen stromu;
Objekt: je součástí hmota který má specifické použití. Příklady: košile, stlačený vzduch, pero, židle.
Mind Map: Matter
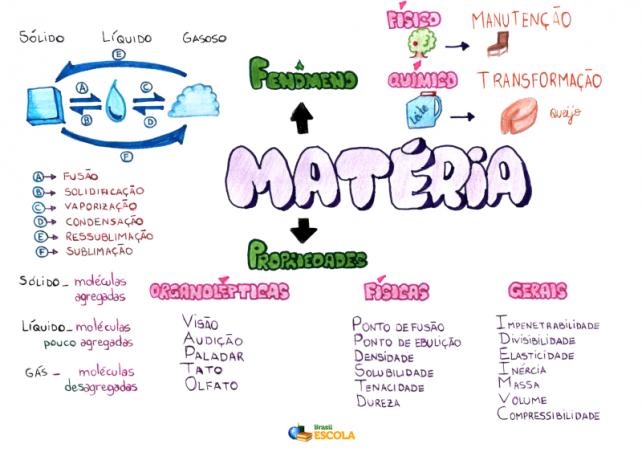
* Chcete-li stáhnout myšlenkovou mapu v PDF, Klikněte zde!
Složení hmoty
Obecně řečeno, všechny hmota je tvořen základní strukturní jednotkou zvanou atom, která má následující složení:
Jádro: složený z protonů a neutronů;
protony: kladně nabité částice;
neutrony: nenabité částice;
Úrovně energie: regiony, kde se nacházejí podúrovně;
Energetické úrovně: regiony, kde jsou orbitaly;
Orbitály: oblasti, kde jsou elektrony s největší pravděpodobností nalezeny;
elektrony: záporně nabité částice.
Když se dva nebo více atomů spojí, vytvoří molekuly, které se mohou tvořit látky stejně jako jednotlivé atomy.
fyzikální stavy hmoty
Vy fyzikální stavy nejběžnější, ve kterých hmotu najdeme, jsou:
Pevný: stav, ve kterém částice (atomy nebo molekuly), které tvoří hmotu, představují nejvyšší úroveň organizace;
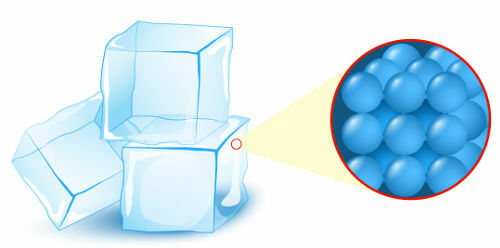
Reprezentace organizace částic v pevném stavu
Kapalný: stav, ve kterém částice (atomy nebo molekuly), které tvoří hmotu, představují nižší úroveň organizace;
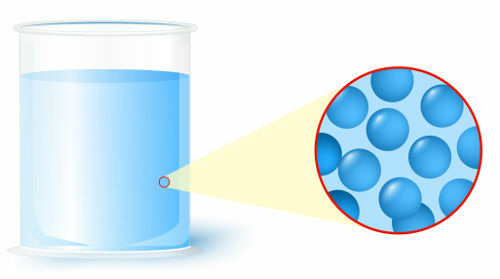
Reprezentace organizace částic v kapalném stavu
Plynné: stav, ve kterém částice (atomy nebo molekuly), které tvoří hmotu, nemají žádnou organizaci.
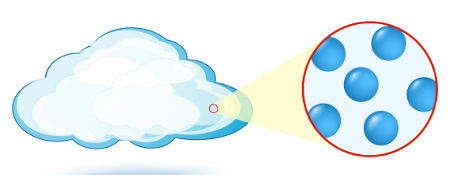
Reprezentace organizace částic v plynném stavu
Obecné vlastnosti hmoty
všechny a všechny hmota, bez ohledu na chemické prvky které ho tvoří, musí mít vlastnosti uvedené níže:
Pružnost: vlastnost, kterou hmota představuje v pevném stavu, když je vystavena extrémní pružné síle, aniž by došlo k porušení jejích struktur. Když tato síla ustane, hmota se vrátí do své původní podoby;
Stlačitelnost: když je část hmoty v plynném stavu podrobena kompresi, zaujímá menší objem;

Materiál stlačovaný do válce
Setrvačnost: když je hmota v pohybu, má tendenci zůstat v pohybu. Pokud je v klidu, má tendenci zůstat v klidu;
Dělitelnost: hmotu lze rozdělit na menší části;
Neproniknutelnost: dva subjekty nemohou zabírat stejný prostor současně.
Podle mě. Diogo Lopes Dias
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-materia.htm

