Jedna z největších výzev pro každého, kdo se učí chemii, se nazývá elektronická distribuce. To, co v této souvislosti představíme, může značně usnadnit vaše studie týkající se elektronové konfigurace navržené vědcem Linusem Paulingem.
Maximální počet elektronů, které se vejdou do každé vrstvy nebo energetické úrovně, je uveden v tabulce:
Vrstva energetické úrovně Maximální počet elektronů
1. K 2
2. L 8
3. M 18
4. N 32
5 ° O 32
6. P 18
7. Q 8.
Rostoucí pořadí energie podúrovní je pořadí v pořadí úhlopříček. Schéma Linuse Paulinga je uvedeno níže:
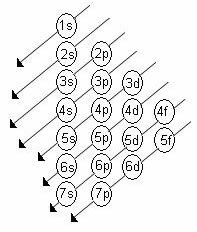
Základní pravidla:
1. Atomové číslo (Z) prvku v neutrálním stavu označuje počet distribuovaných elektronů. Toto číslo je znázorněno v levé dolní části symbolu prvku.
2. Pomocí Paulingova diagramu začněte distribuovat elektrony shora dolů, přičemž vezměte v úvahu rostoucí pořadí energie (orientované ve směru šipek).
3. Naplňte podúrovně maximální úrovní elektronů. Pokud daná podúroveň obsahuje pouze 6 elektronů, nepřekračujte tuto částku.
4. Zkontrolujte počet elektronů jejich sčítáním v každé podúrovni.
Pojďme to uvést do praxe?
Distribuujte elektrony atomu železa (Z = 26).
Pokud je atomové číslo 26, znamená to, že v normálním atomu železa je 26 elektronů. Při použití Paulingova diagramu budeme mít:
Nepřestávejte... Po reklamě je toho víc;)

Líria Alves
Vystudoval chemii
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
FOGAÇA, Jennifer Rocha Vargas. „Pravidla elektronické distribuce“; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/regras-distribuicao-eletronica.htm. Přístup 27. června 2021.