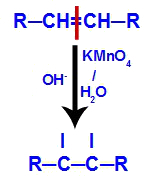
THE mírná oxidace v alkenech je organická reakce prováděná, když je dána alken se umístí do média tvořeného bází s vodou a solí manganistanu draselného (KMnO4), sůl, která se běžně nazývá Bayerovo činidlo.
Vzniklý produkt se nazývá alkohol vicinální, to znamená alkoholy, které mají dvě hydroxylové skupiny (OH-) umístěné na sousedních uhlících, jako v následujícím obecném vzorci:
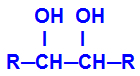
POZNÁMKA: R může být radikál nebo atomy vodíku.
Bayerovo činidlo
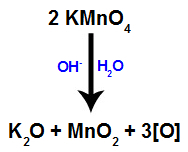
Když Bayerovo činidlo (KMnO4) se smísí s vodou v přítomnosti anorganické báze (OH-), reaguje a tvoří oxid draselný (K.2O), oxid manganičitý (MnO2) a rodící se kyslíky (volný kyslík, reprezentovaný [O]). Podívejte se na vyváženou rovnici procesu.

Tyto rodící se kyslíky vytvořené z Bayerova činidla jsou zodpovědné za mírnou oxidační reakci v alkenech (jak uvidíme v následujících položkách).
Mechanismy mírné oxidační reakce v alkenech
1. mechanismus: tvorba rodících se kyslíků z Bayerova činidla;
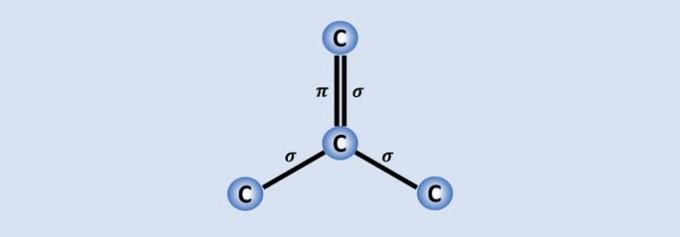
2. mechanismus: Útok rodících se kyslíků na dvojnou vazbu přítomnou v alkenu, což způsobuje narušení pi vazba a následná tvorba volné valence v každém z uhlíků zapojených do pí odkaz.
3. mechanismus: Vznikající kyslíky se spojují s hydroniemi (H+) vytvořený samoionizací vody za vzniku hydroxylových skupin (OH-).
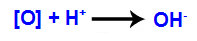
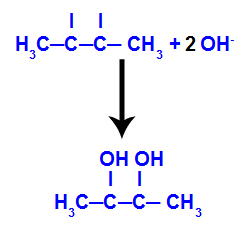
4. mechanismus: Spojení hydroxylových skupin vytvořených v každé z volných valencí umístěných na uhlících, kde byla vazba pí, vznikající vicinálním dialkoholem.

Nepřestávejte... Po reklamě je toho víc;)
Příklady mírných oxidačních reakcí v alkenech
→ Mírná oxidační reakce na but-2-en
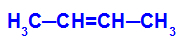
Strukturní vzorec but-2-enu
Zpočátku je dvojná vazba mezi uhlíky 2 a 3 alkenu narušena útokem rodících se kyslíků a vytváří volnou valenci (vertikální stopu) na uhlících 2 a 3.

Přerušení vazby pí mezi uhlíky 2 a 3 v but-2-enu
Poté se rodící se kyslík spojí s hydroniem (H+) z ionizace vody za vzniku hydroxylových skupin (OH-), které se váží na volné valence uhlíků 2 a 3, což vede k vicinálnímu alkoholu.
Vinný alkohol vznikl z but-2-enu
→ Mírná oxidační reakce na 2-methylpropenu
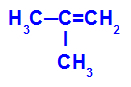
Strukturní vzorec 2-methylpropenu
Zpočátku je dvojná vazba mezi uhlíky 1 a 2 alkenu narušena útokem rodících se kyslíků a vytváří volnou valenci (vertikální stopu) na uhlících 1 a 2.
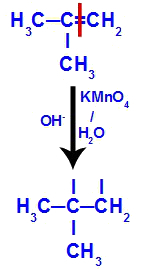
Přerušení vazby pí mezi uhlíky 1 a 2 ve 2-methylpropenu
Poté se rodící se kyslík spojí s hydroniem (H+) z ionizace vody za vzniku hydroxylových skupin (OH-), které se váží na volné valence uhlíků 1 a 2, což vede k vicinálnímu alkoholu.
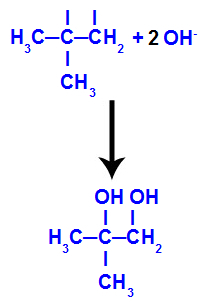
Vinný alkohol vzniklý z 2-methylpropenu
Podle mě. Diogo Lopes Dias
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
DNY, Diogo Lopes. „Mírná oxidace v alkenech“; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/oxidacao-branda-alcenos.htm. Zpřístupněno 28. června 2021.
Chemie

Hydroxylová funkční skupina, primární alkoholy, sekundární alkoholy, terciární alkoholy, methanol, glycerol, ethanol, příprava nitroglycerinu, výroba barev, výroba alkoholických nápojů, kyselina octová, palivo automobily.