Disociace základny to je fyzický proces které se vyskytují u této důležité skupiny anorganických látek, když jsou rozpuštěny ve vodě, nebo když procházejí procesem fúze (průchod z pevného stavu do kapalného stavu skrz topení).
Obecně platí, že fenomén disociace báze je to uvolňování kationtů a aniontů, které tvoří iontová sloučenina, což je v tomto případě základna. Takže během disociace báze, vydání ionty které již ve sloučenině existují, to znamená, že nevznikají žádné nové ionty.
Bázu tvoří jakýkoli kov (X), který je kationtem sloučeniny, nebo amonný kation (skupina NH4+), vázané na hydroxidový aniont (představovaný skupinou OH), jak je znázorněno níže:
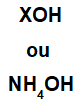
Obecná vyjádření základního vzorce
forma představují disociace báze děje se to pomocí rovnice, ve které v reaktantu máme bázi a v produktech máme ionty (kationty a anionty). Rozdíl je v tom, jak probíhá disociace:
Rozpuštění báze ve vodě:
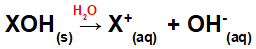
Rovnice představující disociaci báze ve vodném médiu
Disociace základním sloučením:
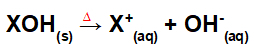
Rovnice představující disociaci báze fúzním procesem
Analýzou výše uvedených obecných rovnic ověříme, že ve všech z nich vždy budeme mít bázi, kation (což je kov nebo NH skupina)4+) a anion (OH-). Ale jsou všichni takoví? Není mezi nimi žádný rozdíl? Na první otázku je odpověď ne a na druhou otázku ano.
Když provádíme disociace od základny, je zásadní nejprve analyzovat základní vzorec, protože z něj můžeme určit zatížení kation a molární množství hydroxidových aniontů, protože molární množství kationtu je standardní (vždy 1 mol).
Je třeba si uvědomit, že množství skupin OH přítomných ve vzorci báze určuje náboj kationtu a množství molů hydroxidového aniontu při disociaci báze.
Podívejme se na příklady hydroxidu hlinitého [Al (OH)3] a hydroxid zlata (AuOH). Ve vzorci na bázi hliníku existují tři skupiny OH a ve vzorci na bázi zlata pouze jedna skupina OH. Při disociaci těchto bází tedy máme:
Al (OH) disociace3:
Protože tato báze má ve vzorci tři OH skupiny, bude náboj na kationtu +3 a množství v molech aniontů se rovná 3 molům, jak vidíme v následující rovnici:
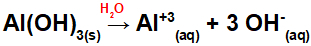
Rovnice disociace hliníkové báze ve vodném prostředí
Disociace od AuOH:
Protože tato báze má ve vzorci skupinu OH, náboj na kationtu bude +1 a množství v molech aniontů se rovná 1 mol, jak vidíme v následující rovnici:
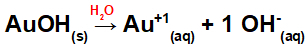
Rovnice disociace báze se zlatem ve vodném prostředí
Podle mě. Diogo Lopes Dias
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-dissociacao-das-bases.htm

