V mnoha léčivých přípravcích a tekutých a pevných potravinářských výrobcích, jako je například ocet a sušenky, se obsah v procentech hmotnosti rozpuštěné látky (m1) ve vztahu k hmotnosti celého řešení (m = m1 + m2). Tato velikost se nazývá Název (T) nebo hmotnostní procento řešení.
Jeho definici lze vyjádřit takto:

Jeho výpočet se tedy provádí pomocí níže uvedené matematické rovnice:
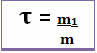
nebo

Jelikož jmenovatel i čitatel jednají se stejnou jednotkou (jednotkou hmotnosti je gram - g), nemá nadpis žádnou jednotku a je menší než 1.
Pokud tedy řekneme, že název daného řešení je 0,4, znamená to, že pro každou jednotku hmotnosti roztoku odpovídá 0,4 hmotnosti rozpuštěné látky. Název je však často vyjádřen v procentech. Chcete-li to provést, jednoduše vynásobte nalezenou hodnotu 100%. V tomto případě se to nazývá Hmotnostní procento (T%) *
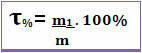
Všimněte si obrázku níže, kde je uveden hmotnostní procentní podíl chloridu sodného ve fyziologickém roztoku:

Fyziologický roztok používaný při léčbě dehydratace obsahuje 0,9% hmotnostního chloridu sodného
V tomto případě to znamená, že na každých 100 g nebo 100 jednotek tohoto roztoku připadá 0,9 g nebo 0,9% solutu, tj. Chloridu sodného (NaCl - stolní sůl).
Dalším příkladem je ocet: na jeho etiketě je údaj, že při jeho přípravě bylo použito 5% hmotnosti kyseliny octové, to znamená, že na každých 100 g roztoku je 5 g této kyseliny.

Název může být uveden také v objemové procento. V tomto případě je jediný rozdíl v tom, že místo vztahu hmotnosti rozpuštěné látky k hmotnosti roztoku; objem rozpuštěné látky souvisí s objemem roztoku podle následujícího vzorce:
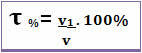
Například v případě běžného alkoholu, který má objemové procento 96%, ve 100 ml roztoku je 96 ml alkohol.

* Termín „Název“ je více používán mezi vědci, zatímco technici a několik autorů knih používají výraz „Mass Percentage“ častěji.
Autor: Jennifer Fogaça
Vystudoval chemii
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/titulo-ou-porcentagem-massa.htm
