Elektrolýza vody spočívá v rozkladu této látky pomocí elektrického proudu a přidání elektrolytu. Pojďme lépe pochopit, jak se to děje?
Přečtěte si také: Co je to elektrolýza?
Jak probíhá elektrolýza vody?
Molekuly vody jsou schopné samoionizace a vytvářejí ionty H.+ (nebo H3Ó+) a oh-:
H2O ↔ H+ + OH-
nebo
2 hodiny2O ↔ H3Ó+ + OH-
Nicméně, voda je velmi slabý elektrolyt a přestože tyto ionty má, nemůže se chovat elektrický proud. K provedení jeho elektrolýzy, tj. Jeho rozkladu pomocí elektrického proudu, je tedy nutné přidat elektrolyt, iontovou solut, kterou může být sůl, báze nebo kyselina.

Prioritní objednávka pro selektivní vybíjení
Jak je však vysvětleno v textu Vodná elektrolýza, v tomto případě nebudeme mít pouze ionty pocházející z vody, ale také ionty látky, která byla v ní rozpuštěna. Při elektrolýze se na elektrodě vybije pouze jeden kation a jeden anion, to znamená, že selektivní vybíjení podle prioritního pořadí.
Aby tedy katoda a anoda, které budou vypouštěny, byly vodou a nikoliv rozpuštěnou látkou, je nutné zvolit
kyselina, báze nebo sůl, jejíž ionty se z elektrod vylučují méně snadno než ionty ve vodě. K tomu je třeba konzultovat prioritní frontu uvedenou níže: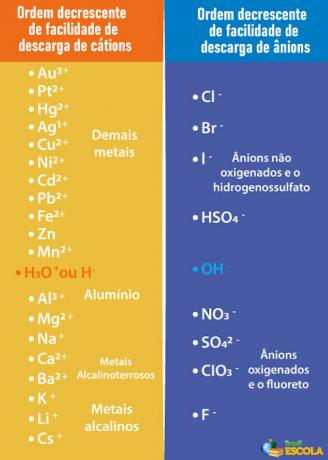
Všimněte si, že kationty uvedené pod H+ mají menší vykládku než ony. V tabulce vpravo vidíme, že anionty pod OH- mají menší snadnost vykládky. Můžeme tedy zvolit například sůl, zásadu nebo kyselinu, která tvoří ionty Na.+, K.+, NA3-, POUZE42- a tak dále, kromě toho, že také tvoří stejné ionty jako voda, tj. H+ a oh-. Některé příklady jsou: kyselina sírová (H2POUZE4), hydroxid sodný (NaOH) a dusičnan draselný (KNO3).
Příklad s reakcemi, které se vyskytly při elektrolýze vody
Řekněme, že elektrolýza vody se provádí přidáním kyseliny sírové. V tomto případě budeme mít uprostřed formaci následujících iontů:
Disociace kyseliny: 1 H2POUZE4 → 2 H+ + 1 SO42-
Autoionizace vody: H2O → H+ + OH- nebo 2 hodiny2O → H3Ó+ + OH-
Jediným existujícím kationtem je H.+, takže je to on, kdo utrpí redukci (zisk o elektrony) na záporné elektrodě (katodě) a bude produkovat plynný vodíkÓ (H2).
Když už mluvíme o aniontech, uprostřed jsou dva aniony, které jsou OS42- a oh-. Jak ukazuje tabulka výše, OS42- je reaktivnější a méně snadno se vybije. Tedy OH- se vybije, oxiduje (ztrácí elektrony) v kladné elektrodě (anodě) a bude produkovat plyn kyslík(Ó2):
Polohodina katody: 4 H3Ó+ + 4 a- → H2O + H2
Anoda s poloviční reakcí: 4 OH- → 2 H2O + 1 O2 + 4 a-
Po přidání celého tohoto procesu se dostaneme ke globální rovnici:
Ionizace vody: 8 H2O → 4 H3Ó+ + 4 OH-
Polohodina katody: 4 H3Ó+ + 4 a- → 4 H2O + 2 H2
Anoda s poloviční reakcí: 4 OH- → 2 H2O + 1 O2 + 4 a-
Globální rovnice: 2H2O → 2 H2 + 1 O.2
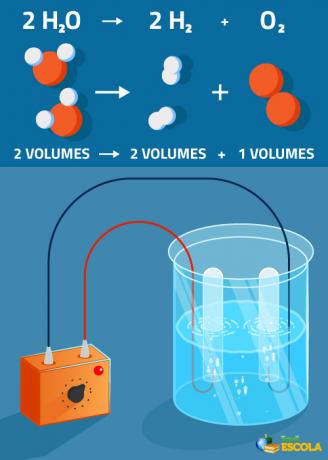
Všimněte si, že objem vyrobeného vodíku je dvakrát větší než objem kyslíku. V praxi však tento přísný poměr není ověřen, protože kyslík je rozpustnější než plyn vodík.
Přečtěte si také: Získávání hliníku elektrolýzou
Aplikace elektrolýzy vody
Elektrolýza vody je velmi důležitý proces, protože vodík je plyn, který lze použít jako palivo. Jako paliva získaná z ropy nejsou obnovitelné, plynný vodík by se mohl stát důležitou alternativou.
Kromě toho již existují způsoby výroby benzinu, které využívají proces elektrolýzy vody. Podívejte se, jak se to děje v textu Vědci mohou z oxidu uhličitého udělat benzín.
Autor: Jennifer Fogaça
Učitel chemie
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/eletrolise-agua.htm
