K dusíkové funkce jsou skupinou organické sloučeniny které mají atomy dusík připojený k uhlíkovému řetězci. Vyznačují se svými příslušnými funkčními skupinami, což jsou soubory atomů spojených v určité konfiguraci a které definují charakteristické vlastnosti každé funkce.
Funkce dusíku jsou:
aminy;
amidy;
nitrosloučeniny;
nitrily;
isonitrily.
Přečtěte si také:Jaké jsou funkce kyslíku?
Shrnutí funkcí dusíku
Dusíkové funkce jsou organické sloučeniny, které obsahují atomy dusíku.
Aminy, amidy, nitrosloučeniny, nitrily a isonitrily jsou funkcemi dusíku.
Anorganické funkce se rozlišují podle funkční skupiny.
Aminy jsou odvozeny substitucí vodíky amoniaku alkylovými radikály.
Amidy mají stejný atom uhlíku spojený s dusíkem a uhlíkem. kyslík.
Nitrosloučeniny obsahují skupinu -NO.2.
Nitrily se vyznačují přítomností trojné vazby mezi uhlíkem a dusíkem.
Izonitrily mají trojnou vazbu mezi dusíkem a uhlíks dusíkem připojeným k uhlíkovému řetězci.
Video lekce o dusíkatých funkcích
Jaké jsou funkce dusíku?
Dusíkové funkce jsou množinou
organické funkce, které mají ve své struktuře atom dusíkukromě atomů uhlíku a vodíku. Jsou to: aminy, amidy, nitrosloučeniny, nitrily a isonitrily,To, co odlišuje dusíkaté funkce, jsou příslušné funkční skupiny, které jsou strukturním uspořádáním atomů odpovědných za vlastnosti látky.
Jaké jsou funkce dusíku?
aminy
Organická funkce důl Je charakterizován vazbou alespoň jednoho uhlíkového řetězce na atom dusíku. Funkční skupina aminů je -N-R1R2R3 (skupiny R jsou uhlíkové řetězce nebo atomy vodíku, z nichž alespoň jeden je uhlíkový řetězec).

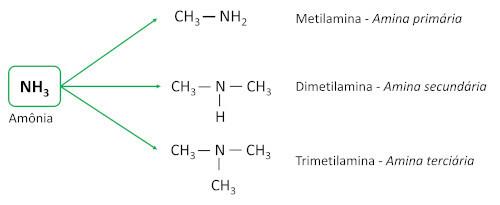
aminy jsou odvozeny od amoniaku (NH3), s jedním nebo více atomy vodíku nahrazenými atomy uhlíku nebo alkylovými ligandy. Jsou to základní látky, opouštějí pH větší než 7 ve vodném roztoku.
Jsou klasifikovány podle množství atomů vodíku nahrazených uhlíkovými ligandy (alkylové nebo arylové skupiny), které se nazývají substituenty.
- Primární aminy: mají jeden uhlíkový substituent.
- Sekundární aminy: mají dva uhlíkové substituenty.
- Terciární aminy: mají tři uhlíkové substituenty, to znamená, že atom dusíku již není vázán k žádnému atomu vodíku, čímž vznikly tři Spojení jednoduché s atomy uhlíku.
A nomenklatura pro aminy dodržuje pokyny IUPAC (Mezinárodní unie čisté a aplikované chemie). V případě primárních aminů se při konstrukci názvu bere v úvahu počet uhlíků (předpona), charakter vazby mezi uhlíky (infix) a používá se termín důl pro koncovku (konec slova).

Viz příklad:
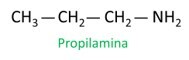
Při přiřazování čísel uhlíkům pro umístění radikálů přiřaďte nejnižší možné číslo atomu, který je nejblíže skupině NH.2.
Pro sekundární a terciární aminy nomenklatura uvažuje nejdelší substituční skupinu připojenou k dusíku jako hlavní řetězec a ostatní ligandy jsou zapsány s předponou odkazující na počet uhlíků a příponou -il, s písmenem N před nimi.

Příklad:
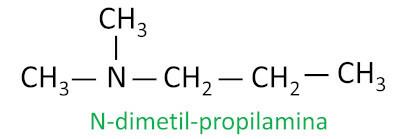
Amidy
Organická funkce amid je charakterizováno navázání karbonylové skupiny (C=O) na atom dusíkukde dusík může být navázán na atomy uhlíku nebo vodíku.
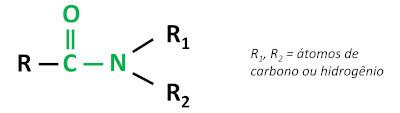
amidy jsou základní látkys ponecháním pH nad 7 ve vodném roztoku. Látka močovina patří do skupiny amidů a je to sloučenina přirozeně se vyskytující v moči, pocházející z degradačních procesů probíhajících v živých organismech.
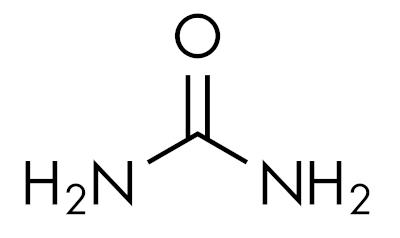
Amidy jsou charakteristické v závislosti na úrovni substituce dusíku. Takhle:
- Primární amidy: drží dva atomy vodíku pohromadě s dusíkem.
- Sekundární amidynebo monosubstituované: jeden z vodíků byl nahrazen uhlíkový řetězec, takže dusík udržuje jednoduchou vazbu s vodíkem.
- terciární amidynebo přemístěny: Dusík již nemá vodíkové vazby, všechny byly nahrazeny uhlíky.

Amidy jsou Pojmenováno podle IUPAC, molekuly jsou pojmenovány podle sekvence:

U rozvětveného amidu se atom uhlíku amidové skupiny účastní hlavního řetězce a počet uhlíků musí začínat u něj. Dívej se:
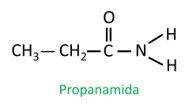 |
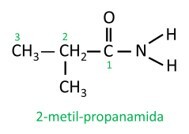 |
V monosubstituovaných nebo disubstituovaných amidech, písmeno N označuje polohu větve který je připojen k atomu dusíku. Pokud je v řetězci další radikál, bude zapsán po identifikaci radikálu odkazujícího na N.
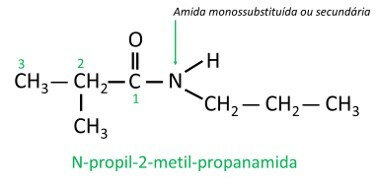
nitrosloučeniny
Vy nitrosloučeniny jsou organické sloučeniny, které obsahují nitroskupinu (-NO2) připojený k uhlíkovému řetězci, které mohou být alifatické (otevřené nebo lineární) nebo aromatické.
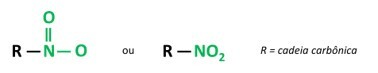
A hlavní charakteristikou těchto látek je jejich výbušná síla. Výbušná kapacita je spojena s aromatickými nitrosloučeninami a čím větší je počet nitroskupin, tím větší je výbuch. Alifatické nitrosloučeniny se používají v laboratořích jako organická rozpouštědla.
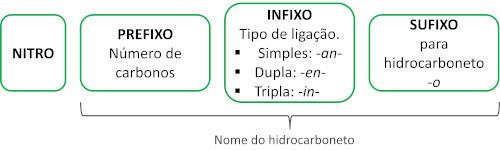
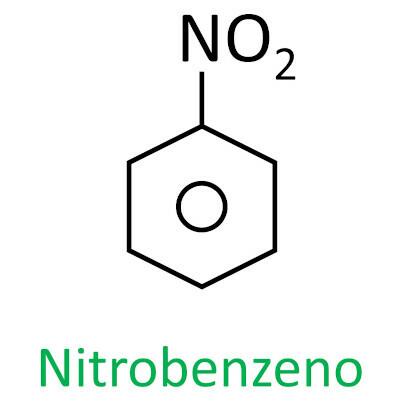
Názvosloví pro tyto sloučeniny je tvořeno slovem nitro následovaný jménem uhlovodík (předpona + infix + koncovka -Ó).
Podívejte se na některé příklady:
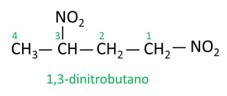 |
 |
nitrily
Nitrily jsou organické sloučeniny vyznačující se tím trojná vazba mezi atomem uhlíku a atomem dusíku, představující funkční skupinu – C ≡ N. V nitrilech je dusík na konci a uhlík je připojen přímo k uhlíkovému řetězci.

nitrily Také známý jako kyanidy, protože pocházejí z reakcí s kyselinou kyanovodíkovou (HCN).
jsou to látky toxický pro lidi, protože v těle mohou tvořit kyselinu kyanovodíkovou v kontaktu se žaludeční kyselinou, čímž brání procesům buněčné dýchání buněk.
V přírodě se nitrily vyskytují v některých peckovinách, ale ve velmi nízké koncentraci, která nepředstavuje riziko, a v listech divokého manioku.

Iupacovo pravidlo pro nomenklaturu nitrilů definuje tento termín nitril přidat jako příponu:

Podívejte se na některé příklady:
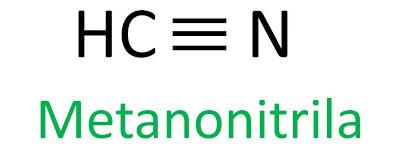 |
 |
Obvyklá forma nomenklatury pro nitrily je kyanid + radikální název.
isonitrily
Isonitrily nebo isonitrily jsou sloučeniny tvořené trojná vazba mezi atomem uhlíku a atomem dusíku, představující funkční skupinu – R ≡ C. V isonitrilech je uhlík na konci a dusík je připojen přímo k uhlíkovému řetězci.

Isonitrily se liší od nitrilů polohou atomů dusíku a uhlíku a V isonitrilech je dusík charakterizován jako heteroatom., protože je umístěn mezi dvěma uhlíky.
Jsou to nestabilní druhy a při zvýšených teplotách se mohou přeměnit na nitrily. Reakce kyseliny isokyanidové vedou ke vzniku isonitrilů, a proto jsou tyto sloučeniny také známé jako isokyanidy.
Izonitrilové molekuly se řídí Iupacovým pravidlem pro pojmenování:
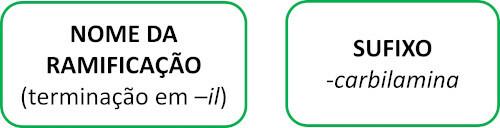
Podívejte se na některé příklady:
 |
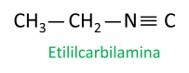 |
Aplikace funkcí dusíku
Látky náležející k dusíkatým funkcím mají četné aplikace, zejména v průmyslové oblasti, pro výrobu polymery, pryž, syntetická vlákna, léčiva, agrochemikálie, pesticidy a výbušniny.
K aminy se používají při výrobě barviv, mýdla, drogy, v procesu vulkanizace pryže, výbušniny a další průmyslové procesy a nacházejí se také v rostlinách a vznikají při procesech rozkladu organické hmoty.

K amidy mají široké uplatnění v průmyslovém a chemickém sektoru, které jsou přítomny při výrobě polymerů (jako je nylon a polyuretan), pryskyřic, výbušnin, hnojiva, repelenty proti hmyzu, hnojiva a léky.

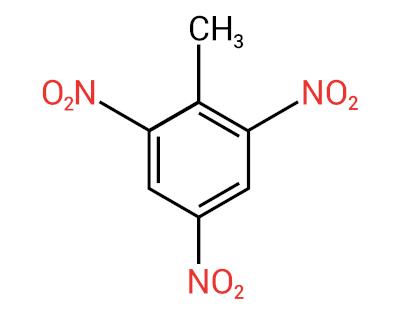
Vy nitrosloučeninyJeho hlavní aplikací je výroba výbušnin. které se používají ve vojenském, průmyslovém a hutním sektoru (k těžbě surovin). Jednou z nejznámějších nitrosloučenin je trinitrotoluen, lidově známý jako TNT. Další aplikace nitrosloučenin jsou při výrobě pesticidybaktericidy, barviva, rafinace ropy atd.

K nitrily se používají jako organická rozpouštědla v laboratoři a v průmyslu, podílí se na těžbě a výrobních procesech některých syntetických vláken, plastových polymerů, barviv a hnojiv.

K isonitrily se používají v různých procesech výroby organických sloučenin, jako jsou rozpouštědla, a podílejí se na výrobě agrochemikálií, pesticidů, kaučuků a plastů.
Přečtěte si také:Halogenidy — látky, které mají atomy halogenu připojené k uhlíkovému řetězci
Řešená cvičení o funkcích dusíku
Otázka 1
(FPS-PE-modified) Aplikace dusíkatých sloučenin v syntetické organické chemii je velmi rozmanitá a zahrnuje přípravu léčiv, barviv, výbušnin a vitamínů. Podívejte se na sloučeniny níže.
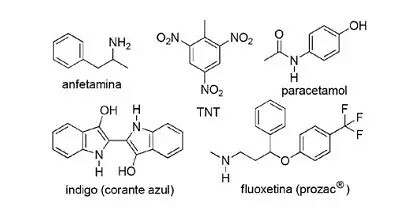
O těchto sloučeninách označte nesprávné tvrzení.
a) TNT je nitrosloučenina.
b) Dusíkatá část fluoxetinu je sekundární amin.
c) Amfetamin je klasifikován jako primární amid.
d) Indigo má ve své struktuře heteroaromatické kruhy.
e) Dusíkatá část paracetamolu je amid.
Rozlišení:
Dopis C
Položka The je správně, protože TNT je nitro sloučenina, protože nemá žádné skupiny2.
Položka B je správně. Dusíkatá část fluoxetinu je sekundární amin, protože je spojen se dvěma uhlíkovými segmenty.
Položka w je nesprávný, protože amfetamin je klasifikován jako primární amin, nikoli amid. Všimněte si, že přítomná skupina je NH2. Takže toto je podstata otázky.
Položka d je správné, protože indigo má ve své struktuře heteroaromatické kruhy, to znamená kruhy tvořené atomy uhlíku a dalším prvkem — v tomto případě dusíkem.
Položka to je je správný, protože paracetamol je amid, představující uhlík spojený s dusíkem a kyslíkem.
otázka 2
(UFMS) Yerba mate (Ilex paraguariensis), původem z Jižní Ameriky, se používá jako tonikum a povzbuzující nápoj. K přípravě lze použít produkt získaný zpracováním listů yerba maté chimarrão a tereré, mimo jiné nápoje běžně a kulturně konzumované v regionech Argentiny, Paraguaye a Brazílie. Velký zájem o yerba maté je způsoben přítomnými chemickými sloučeninami díky svým antioxidačním, stimulačním a diuretickým vlastnostem.
(K dispozici v: http://repositorio.utfpr.edu.br/jspui/bitstream/1/3158/1/PG_PPGEP_Henrique%2C%20 Flavia%20Aparecida_2018.pdf. Přístup dne: 1. listopadu. 2018. Přizpůsobeno).
Stimulační vlastnosti yerba maté souvisí s obsahem methylxanthinů, z nichž jedním z hlavních je kofein, struktura uvedená níže:

Při analýze strukturního vzorce kofeinu je správné uvést, že má následující organické funkce a vlastnosti:
a) aldehyd a amid, zásadité.
b) amin a amid, alkalické.
c) amin a keton, alkalické.
d) keton a amid, amfoterní.
e) karboxylová kyselina a amin, zásadité.
Rozlišení:
Písmeno B
Analýzou kofeinové struktury jsou identifikovány aminové a amidové funkční skupiny, jak je zvýrazněno na obrázku níže. Protože tyto dvě skupiny mají bazickou nebo alkalickou charakteristiku, kofein má také tuto charakteristiku, což znamená, že vodné roztoky kofeinu mají pH nad 7.
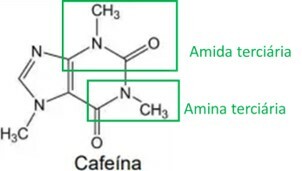
Autor: Ana Luiza Lorenzen Lima
Učitel chemie
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/funcoes-nitrogenadas.htm

