THE hassium, se symbolem Hs a protonové číslo 108, je jedním z prvků známých jako transaktinidy. Stejně jako všechny prvky této skupiny se nevyskytuje v přírodě, protože je syntetický, kromě toho je radioaktivní a nestabilní. Jeho syntéza je připisována německým laboratořím Helmholtzova centra pro výzkum těžkých iontů (GSI) ve městě Darmstadium v Německu a jeho jméno bylo dáno na počest německého státu Hesensko, který se nachází v centrální oblasti rodiče.
Hassium je nejtěžší prvek, jehož vlastnosti jsou analyzovány prostřednictvím experimentů prováděných samotným GSI. Výsledky byly důležité pro potvrzení pozice Hs v Periodická tabulka, protože podobnost mezi tímto prvkem a osmiem a rutheniem, lehčími prvky skupiny 8, byla vnímána.
Přečtěte si také:Bohrium — syntetický chemický prvek pojmenovaný po Nielsi Bohrovi
Hassium Shrnutí
Je to syntetický chemický prvek nacházející se ve skupině 8 periodické tabulky.
Byl syntetizován Gesellschaft für Schwerionenforschung (GSI) v Darmstadiu v Německu.
Je to a radioaktivní prvek a nestabilní.
Teoretická a experimentální data potvrzují, že svými vlastnostmi připomíná nejlehčí prvky své skupiny.
Jako transaktinid nemůže být produkován ve velkém měřítku, kromě toho, že je produkován rychlostí několika atomy.
Vlastnosti hassia
Symbol: hs
Protonové číslo: 108
Atomová hmotnost: 277 c.u.
Elektronická konfigurace: [Rn] 7s2 5f14 6d6
Nejstabilnější izotop: 269Hs (14 sekund poločas)
Chemická řada: skupina 8; transaktinidy; super těžké prvky.
Vlastnosti Hassium
Hassium je a syntetický prvek a nejtěžší ze skupiny 8. Považuje se za a transactinid, právě proto, že se objevuje v periodické tabulce po sérii aktinidů. Jako všechny transaktinidy je hassium prvkem radioaktivní a nestabilní.
To znamená, že jeho izotopy dosahují málo času poločas rozpadu (doba potřebná k tomu, aby hmotnost atomového druhu klesla na polovinu). V současné době je známo sedm izotopů hassia, jejichž hmotnost se pohybuje od 264 do 270 hodin. Mezi všemi je nejstabilnější izotop 269Hs, s poločasem rozpadu 14 sekund.
Přestože krátký poločas ztěžuje studium chemických vlastností transaktinidů, hassium mělo v tomto ohledu o něco více štěstí. V červnu 2001 bylo oznámeno, že se stal nejtěžší prvek, jehož vlastnosti jsou analyzovány.
Týmu se podařilo ve městě Darmstádio v Německu vyrobit asi šest atomů Hs s poločasem rozpadu přibližně 10 sekund. I když se to zdá málo, stačilo to k potvrzení, že jde o oxid hassitý, HsO4, má silné podobnosti s oxidy lehčích prvků skupiny 8, RuO4 a OsO4, toto je ruthenium to je osmium.
Viz také: Seaborgium — další syntetický chemický prvek s radioaktivními vlastnostmi a krátkým poločasem rozpadu
Získání Hassia
Transaktinidy mají společnou obtížnost při výrobě. Obecně je vyžadováno nejmodernější vybavení jako např urychlovače částic. V nich se iontové druhy srážejí s prvky vysokých atomová hmotnost k vytvoření supertěžkých prvků (ve kterých je zahrnut Hs).
V případě hassia zahrnovaly studie, které potvrdily jeho pozici ve skupině 8 periodické tabulky, jeho výrobu prostřednictvím bombardování hořčíkem-26, přičemž cílem bylo kurium-248.
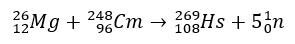
Experimenty s těmito prvky jsou drahé, a proto je běžné, že se provádějí teoretické studie, které přesně vypočítají a předpovídají chemické vlastnosti. Krátký poločas je dalším komplikujícím faktorem.
Experimentální techniky separace a detekce musí být velmi rychlé, aby bylo dosaženo důvěryhodných výsledků. Konečně, reakční účinnost těchto prvků je velmi nízká, pohybuje se v rozmezí několika atomových jednotek.
Preventivní opatření s Hassium
Hs se nevyrábí ve velkém, a proto se s ním manipuluje nezahrnuje rizika. Navíc se získává ve výzkumných centrech s vysoce kontrolovaným prostředím.
historie hassia

Transactinidi byli protagonisty vědeckého sporu kvůli Studená válka, a Válka převodů, název vytvořený v souvislosti se spory, které se týkaly výroby a rozpoznávání prvků po fermiu (Fm, Z = 100). Do tohoto závodu se zapojily laboratoře:
Společný ústav pro jaderný výzkum, ve městě Dubna, Rusko;
Lawrence Berkeley National Laboratory v Berkeley v Kalifornii;
Gesellschaft für Schwerionenforschung (GSI, lépe přeloženo jako Helmholtzovo centrum pro výzkum těžkých iontů) v Darmstadiu v Německu.
V případě prvku 108 se jednalo o skupiny GSI a Dubna. Ačkoli vědci z Dubny (vedení Jurijem Oganessianem) nejprve oznámili přítomnost prvku 108, zásluhu si vzali ti z německé skupiny, protože GSI přinesl přesvědčivější výsledky, zatímco v jednom experimentu se mu podařilo vyrobit tři atomy izotopu 265, zatímco v jiném vyrobil jeden atom izotopu 264.
Tyto izotopy byly vyrobeny pomocí Universal Linear Accelerator (Unilac, lépe přeloženo jako Universal Linear Accelerator), s bombardováním 208Pb by 58Víra. V roce 1997 Mezinárodní unie čisté a aplikované chemie (IUPAC) uznala prvek 108 se symbolem Hs jako Hassium na počest německé spolkové země Hesensko.
Cvičení řešená na hassium
Otázka 1
Hassium, symbol Hs, je považován za nejtěžší prvek, jehož vlastnosti byly experimentálně studovány. V té době byli vědci schopni určit vlastnosti oxidu hasitého, HsO4. U tohoto druhu má Hs stejné NOx jako lehčí prvky své skupiny, osmium (Os) a ruthenium (Ru). Oxidační číslo Hs v oxidu hasitém se rovná:
a) 0
B) +2
C) +4
D) +6
E) +8
Řešení:
Alternativa E
THE kyslík, když v a kysličník, získává náboj rovný -2. Takže NOx z Hs, které budeme nazývat x, lze vypočítat jako:
x + 4(-2) = 0
x - 8 = 0
x = +8
otázka 2
Nejstabilnější izotop hassia, Hs, má poločas rozpadu pouhých 14 sekund. To znamená:
A) za 14 sekund se hmotnost izotopu Hs zdvojnásobí.
B) po 14 sekundách bude hmotnost izotopu Hs menší než polovina původní hmotnosti.
C) za necelou minutu bude hmotnost izotopu Hs 1/16 jeho počáteční hmotnosti.
D) za jednu minutu bude hmotnost izotopu Hs přesně polovina jeho počáteční hmotnosti.
E) za 14 sekund se hmotnost izotopu Hs vydělí 4.
Řešení:
Alternativa C
Poločas rozpadu udává čas potřebný k tomu, aby se množství atomových druhů snížilo na polovinu. To znamená, že každých 14 sekund klesne množství Hs na polovinu. Pozorováním tohoto poločasu rozpadu je jasné, že s 56 sekundami již bylo dosaženo čtyř poločasů rozpadu, což způsobuje, že hmotnost Hs je dělena 2.4, což je 16.
Autor: Stefano Araújo Novais
Učitel chemie
