Alkoholy mohou podléhat oxidaci, jsou-li vystaveny oxidačnímu činidlu, jako je vodný roztok dichromanu draselného (K2Cr2Ó7) nebo manganistan draselný (KMnO4) v kyselém prostředí.
Vznikající kyslík [O] uprostřed napadne uhlík spojený s alkoholovou funkční skupinou (hydroxyl - OH), tvořící velmi nestabilní sloučeninu zvanou twin diol, která má dva hydroxyly spojené se stejným uhlík. Protože je nestabilní, tato sloučenina uvolňuje vodu a dává vzniknout novému produktu.
Tento produkt bude záviset na typu alkoholu, který byl oxidován, ať už jde o primární, sekundární, terciární nebo methanol.
Stručně řečeno, máme:
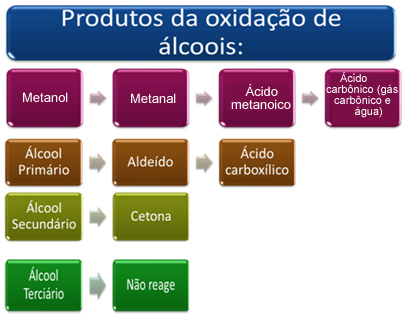
Viz každý případ níže:
- Metanol (H3C─ OH):
Metanol je jediný alkohol, který má tři vodíky vázané na uhlík, který podléhá oxidaci. V tomto případě, protože na molekule jsou tři body, které může nascentní kyslík napadnout, dojde ke třem po sobě jdoucím oxidacím, jak je znázorněno na obrázku níže:
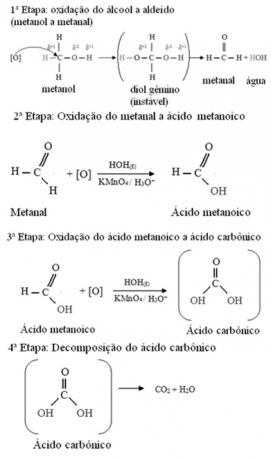
- Primární alkoholy:
V těchto sloučeninách je hydroxylový uhlík spojen pouze s jedním atomem uhlíku, to znamená, že dva další ligandy jsou vodíky a vznikající kyslík má dvě místa, kam může útočit.
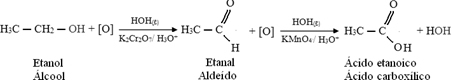
Nejprve dojde ke vzniku aldehydu, jak je ukázáno níže:
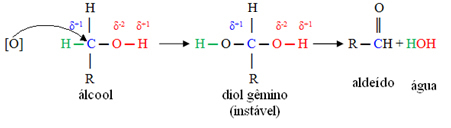
Ale oxidace pokračuje, protože činidla používaná k oxidaci alkoholu jsou silnější než činidla používaná k oxidaci aldehydu. Poté další vznikající kyslík napadá karbonylový uhlík a vytváří karboxylovou kyselinu.
Následuje příklad oxidace ethanolu, nejprve na ethanal a poté na kyselinu ethanovou (kyselinu octovou). Tato celková reakce je přeměna vína na ocet.
Nepřestávej teď... Po reklamě je toho víc ;)
K částečné oxidaci etanolu na ethanal dochází, když alkoholik podstoupí jednorázový dechový test. Uvnitř tohoto zařízení je pevná směs dichromanu draselného a oxidu křemičitého v kyselém prostředí, přičemž dochází k následující reakci:
K2Cr2Ó7 (vod.) + 4H2POUZE4 (vod.) + 3 CH3CH2Ach(G) → Kr2(POUZE4)3 (vod.) + 7 hodin ráno2Ó(1) + 3 CH3CHO(G) + K2POUZE4 (vod.)
oranžovýethanol (bezbarvý)zelenáethanal (bezbarvý)
Všimněte si, že kromě oxidace ethanolu (alkoholu) na ethanal (aldehyd) dochází současně k redukci dichromanu, který je oranžový, na chrom (III), nebo dokonce chrom (II), který je zelený. Změna barvy bude indikovat, že osoba má více alkoholu v krvi, než je povoleno.
- Sekundární alkoholy:
Jedná se o sloučeniny, ve kterých je hydroxylový uhlík vázán na dva další atomy uhlíku a pouze jeden atom vodíku. Proto bude existovat pouze jedno místo v molekule, kde může vznikající kyslík atakovat a vznikne pouze jeden typ produktu, kterým bude vždy keton:
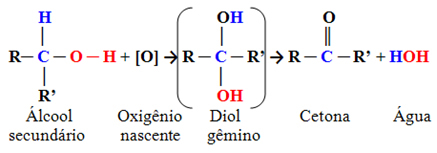
Vzhledem k tomu, že karbonylový uhlík ketonu nemá přímo na sebe navázaný žádný vodík, neexistuje již žádná možnost další oxidace. Reakce se proto zastaví na ketonu.
- Terciární alkoholy:
Terciární alkoholy jsou ty, ve kterých uhlík, který má -OH skupinu, vytváří tři vazby s jinými atomy uhlíku. Protože se nevážou s vodíky, není na molekule žádný bod, který by mohl být napaden vznikajícím kyslíkem. Díky této skutečnosti nepodléhají terciární alkoholy oxidaci.
* Zdroj a autor obrázku: CostaPPPR.
Autor: Jennifer Fogaça
Vystudoval chemii
Chtěli byste odkazovat na tento text ve školní nebo akademické práci? Koukni se:
FOGAÇA, Jennifer Rocha Vargas. "Oxidace alkoholů"; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/oxidacao-dos-alcoois.htm. Zpřístupněno 27. července 2021.
Chemie

Jak funguje dechový analyzátor, koncentrace alkoholu, dechový analyzátor, reakce zahrnující etylalkohol, druhy dechové analyzátory, dichroman draselný, palivový článek, katalyzátor, uvolňování elektronů, kyselina octová, vodík, konc