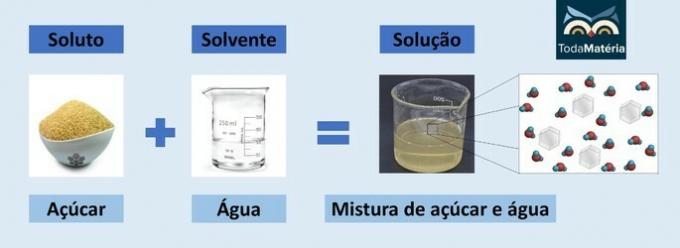
Koloidy, koloidní roztoky nebo koloidní systém jsou směsi, které mají vzhled roztoku, tj. Homogenní směsi. Ve skutečnosti však jde o heterogenní směsi.
Je tomu tak proto, že i když to není pouhým okem jasné, rozdíl v koloidních směsích lze pozorovat pomocí nástrojů, jako je mikroskop.
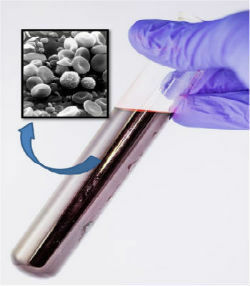 Krev, i když se zdála být homogenní, pomocí mikroskopu jsme zjistili, že je složena z několika složek.
Krev, i když se zdála být homogenní, pomocí mikroskopu jsme zjistili, že je složena z několika složek.
Koloidy jsou přítomny v našem každodenním životě. Oni jsou příklady koloidů: zvlhčovací krém, jogurt, mléko, krev, barviva a džem.
Z tohoto důvodu některé chemické produkty naznačují, že musí být před použitím protřepány. To je třeba udělat, aby se spojily koloidní částice.
Koloidní směsi se zároveň neusazují přirozeně. Pokud vložíme koloid do nádoby, částice se neusadí na dně. Nelze je také filtrovat.
Velikost částic přítomných v koloidech je mezi 1 a 100 nanometry (1 nanometr odpovídá 1 miliontině milimetru).
Všechno mimo tento rozsah je homogenní nebo heterogenní směsi.
Homogenní směsi jsou považovány za skutečná řešení. Jeho částice jsou menší než 1 nanometr. Heterogenní směsi mají částice větší než 100 nanometrů.
Dozvědět se víc o Chemická řešení a Separace směsí.
Jaké jsou vaše vlastnosti?
Složky koloidů se nazývají rozptýlené a dispergační prostředek. Množství dispergátoru je vždy vyšší.
Zjevně předpokládají homogenní směšovací charakteristiku.
Jedním z příkladů je vaječný bílek zbitý na sněhu: bílý v tekuté formě převezme roli rozptýlené složky.
Vzduch, který způsobil, že se bílá změnila na pěnu, je disperzní složkou, protože k dosažení této směsi bylo zapotřebí více vzduchu než bílé.
Koloidy navíc umožňují průchod světla mezi nimi, což u homogenních směsí neplatí.
Pokud míříme baterkou s malým paprskem světla na koloidní směs, je možné vidět paprsek světla procházející celou nádobou, kde se nachází. Tak se tomu říká Tyndallův efekt.
Stejným experimentem je také možné detekovat náhodný pohyb částic ve směsi. Tomu se říká Brownovo hnutí.
Stručně řečeno, vlastnosti koloidních systémů oni jsou:
- Fáze směsi nejsou snadno rozeznatelné;
- Rozsah velikosti částic je 1 a 100 nanometrů;
- Tyndallův efekt;
- Přítomnost dispergovaných částic a dispergátorů;
- Neusazují se přirozeně ani nemohou být filtrovány;
- Brownovo hnutí.
Druhy koloidů
Koloidy se klasifikují podle fyzikálního stavu dispergovaných a dispergujících částic.
Druhy koloidů jsou: aerosol, emulze, pěna, gel a sol (ty, které vypadají jako roztok). Další informace o každém z nich:
Aerosol
Rozptýlená součást: Pevné nebo kapalné
Disperzní komponenta: plyn
Příklady: Kouř, mlha, mrak, sprej
Emulze
Rozptýlená součást: Kapalný
Disperzní komponenta: Kapalné nebo pevné
Příklady: Majonéza, máslo, sýr, zmrzlina
Pěna
Rozptýlená součást: plyn
Disperzní komponenta: Kapalné nebo pevné
Příklady: Šlehačka, bílá ve sněhu, pěna na holení, popcorn
Gel
Rozptýlená součást: Kapalný
Disperzní komponenta: pevný
Příklady: Želatina, silikagel, zubní pasta
slunce
Rozptýlená součást: pevný
Disperzní komponenta: Kapalné nebo pevné
Příklady: Pearl, Ruby, Blood
Chcete-li se dozvědět více, dozvíte se o metodě oddělování koloidních směsí Odstředění.