Nitrační reakce jsou substituční reakce, ke kterým dochází prostřednictvím kyseliny dusičné (HNO3). K tomuto typu reakce dochází zejména s alkany a s benzenem a jeho deriváty, kde je jeden z atomů vodíku připojených k řetězci nebo k aromatickému jádru nahrazen skupinou NO.2, čímž vznikne nitrosloučenina a voda.
Podívejte se na několik příkladů:
1. Nitrace alkanu:
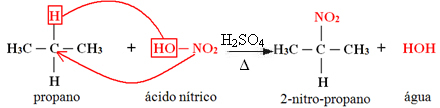
Pokud má alkan více než dva uhlíky, vytvoří se směs různých substituovaných sloučenin. Množství každé získané sloučeniny bude úměrné následujícímu pořadí snadnosti, s jakým se vodík uvolňuje do molekuly:

Ve výše uvedeném případě neexistuje terciární uhlík, existuje pouze jeden sekundární a dva primární; tedy největším množstvím sloučeniny vytvořené jako produkt bude 2-nitro-propan.
Pokud je dostatek kyseliny dusičné, může být jiný vodík nahrazen nitroskupinou, což vede ke vzniku 2-dinitropropanu (struktura níže), sloučenina široce používaná jako přísada do motorové nafty, zvyšuje její oktanové číslo a snižuje emise saze.
NA2
│
H3C─C─CH3
│
NA2
2. Nitrace benzenu:
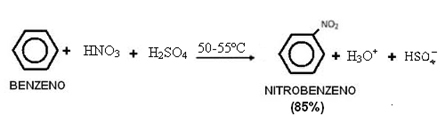
Všimněte si, že k této reakci dochází v přítomnosti tepla, protože benzen se zahřívá se sulfonovou směsí, tj. Koncentrovanou kyselinou dusičnou a koncentrovanou kyselinou sírovou. Kyselina sírová je katalyzátor, který způsobuje, že se reakční rychlost zvyšuje, protože benzen pomalu reaguje s kyselinou dusičnou.
3. Nitrace benzenových derivátů:
V takových případech bude místo substituce záviset na substituční skupině nebo funkční skupině připojené k aromatickému jádru. Texty „Radikály řízení v benzenovém kruhu" a "Elektronické efekty radikálů meta a ortho-to-directors”Vysvětlete více o tom, jak k tomu dochází.
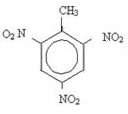
Aromatické kruhy mohou podléhat nitraci a vést k výbušninám. Příkladem je trinitrotoluen (2-methyl-1,3,5-trinitrobenzen), lépe známý jako TNT, a existuje několik pigmentů používaných hlavně v tkaninách.
Autor: Jennifer Fogaça
Vystudoval chemii
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/reacoes-organicas-nitracao.htm


