Sublimace je změna z pevného stavu do plynného stavu a naopak, aniž by prošla kapalným stavem.
Aby látka prošla procesem sublimace, musí podléhat určitým hodnotám teploty a tlaku.
Mothballs a CO2 pevná látka (suchý led) jsou příklady látek, které podléhají sublimaci za okolních podmínek.

Fázový diagram
Můžeme objevit fyzický stav látky tím, že budeme znát hodnoty teploty a tlaku, kterým je vystavena.
K tomu používáme diagramy vytvořené pro každou látku z hodnot zjištěných experimentálně.
Volala "Fázový diagram", je rozdělena do tří oblastí, které představují pevné, kapalné a plynné skupenství. Čáry, které tyto oblasti ohraničují, signalizují body, ve kterých látka mění fázi.
Trojitý bod v diagramu označuje teplotu a tlak, při kterých může látka koexistovat ve třech fázích. Pod tímto bodem je sublimační křivka.
Body na této křivce určují hodnoty tlaku a teploty, při kterých dojde k sublimaci.
Když je pevná látka vystavena tlaku menšímu než trojitý bod, pokud se zahřeje, projde přímo do plynného stavu.
Ke změně z přímého pevného stavu na plynný může dojít také snížením tlaku, když je jeho teplota nižší než teplota trojného bodu.
Více se dozvíte na: Změny fyzického stavu.
Fázový diagram oxidu uhličitého (CO)2 )
Trojitý bod CO2 nastane, když je tlak 5 atm. Tato skutečnost ospravedlňuje, že je běžné vidět výskyt sublimace v suchém ledu, protože okolní tlak je 1 atmosféra.
Z tohoto důvodu se za okolních podmínek nezískává kapalný oxid uhličitý. Za těchto podmínek je buď v pevném stavu, nebo v parním stavu.
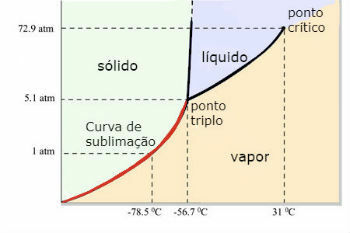
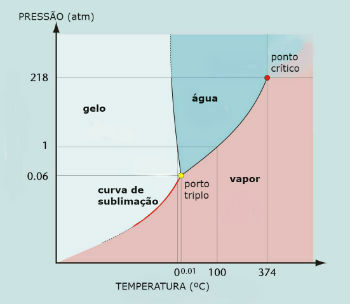
Schéma vodní fáze (H2Ó)
Trojitý bod vody nastává, když je tlak pouze 0,06 atm. Za podmínek prostředí tedy není běžné, že voda sublimuje.
Chcete-li se dozvědět více, přečtěte si také:
- Fyzikální stavy vody
- Fyzické stavy hmoty
- Zkapalnění nebo kondenzace
- Vlastnosti hmoty
- Tuhnutí
- Fúze
- Vypařování
- Vařící
- Vypařování