Na spalovací reakce jsou přítomny v mnoha aspektech našeho každodenního života. Například hlavní zdroje výroby energie jsou výsledkem spalování nebo spalování určitých paliv, jako je například ethanol, benzín, dřevěné uhlí. Energie, kterou potřebujeme k přežití ak práci, je dále výsledkem spalovacích reakcí, které probíhají v našich buňkách, když „spalujeme“ jídlo, které jíme.
Ale co je potřeba k tomu, abyste měli spalovací reakci?
Jsou potřeba tři věci:
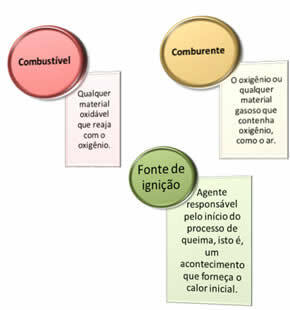
Tyto tři faktory tvoří požární trojúhelník, protože jakmile začne spalovací reakce, uvolněná energie udržuje reakci a umožňuje jí pokračovat, dokud palivo, okysličovadlo nebo teplo (uvolněná energie) nezmizí. To znamená, že bude existovat Řetězová reakce.
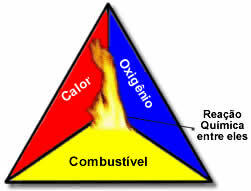
Pokud například někdo hodí zapálenou cigaretu do lesa, dojde k požáru (reakce spalování). V tomto případě Keř to je pohonné hmoty, O kyslík přítomný ve vzduchu atmosférický je okysličovadlo to je cigareta lit byl zdroj vznícení. Toto spalování bude pokračovat, dokud nebude vyloučen jeden ze tří faktorů. Pokud hasiči hodí vodu, teplo bude odstraněno. Ale i když se pro zastavení tohoto hoření neudělá nic, skončí to v určitém okamžiku, to znamená, když dojde palivo (les).
Jak již bylo zmíněno, v těchto reakcích se uvolňuje teplo, takže spalování je exotermická reakce. Tento typ reakce je však neúplné spalování. Abyste pochopili proč, podívejte se na rozdíl mezi úplným a neúplným spalováním:
Nepřestávejte... Po reklamě je toho víc;)
Kompletní spalování:
Při analýze organických sloučenin jako paliv musíme:
| THE úplné spalování nastane to, když je uhlíkový řetězec rozbit a všechny atomy uhlíku v uhlíkovém řetězci jsou úplně oxidovány. |
| Vy tvarované výrobky uhlovodíky bude CO2 (oxid uhličitý) a H2Ó (Voda). |
Sledujte úplné spalování isoctanu, který je jednou ze složek benzínu.
C8H18 (g) +25/2 O.2 (g) → 8 CO2 (g) + 9 hod2Ó(1)
Nedokončené spalování
| V tomto případě není k dispozici dostatek oxidačního činidla, tj. Dostatečné množství kyslíku na spalování veškerého paliva. |
| Takto vzniklé produkty jsou CO (oxid uhelnatý) a H2Ó. |
Pozorujte stejné spalování isoctanu, nyní však neúplně:
C8H18 (g) + 17/2 O.2(G) → 8 CO (G) + 9 hod2Ó(1)
Příkladem je spalování lesů, protože výsledné emise se skládají z CO a určitých látek, jako jsou saze (C), stejně jako popel a další jednoduché a složité organické sloučeniny. Oxid dusíku, ozon a aldehydy mohou také vznikat v důsledku sekundárních reakcí v důsledku přítomnosti dalších složek ve vzduchu.
C8H18 (g) + 9/2 O.2 (g) → 8C (G) + 9 hod2Ó(1)
Autor: Jennifer Fogaça
Vystudoval chemii
Tým brazilské školy
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
FOGAÇA, Jennifer Rocha Vargas. „Úplné a nedokončené spalování“; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/combustao-completa-incompleta.htm. Zpřístupněno 27. června 2021.