entropie je a velikosttermodynamika spojený s nevratnost stavů fyzického systému. To je běžně spojováno se stupněm „porucha“Nebo„náhodnost„Systému. Podle jednoho z prohlášení 2. zákon termodynamiky:
“V tepelně izolovaném systému musí měření entropie vždy časem stoupat, dokud nedosáhne své maximální hodnoty. “
Jinými slovy entropie je schopen měřit význam „šipka času„Systému. Když vidíme obrázky níže, intuitivně víme, že počáteční stav systému je reprezentován obrazem vlevo, odjetz největších organizace:
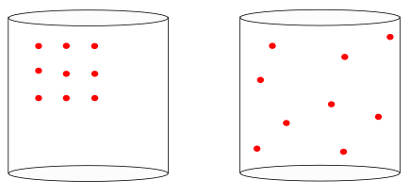
Při pohledu na předchozí obrázek víme, že nejpravděpodobnější konečnou konfigurací je konfigurace, ve které mají atomy rychlosti ve všech směrech, jakož i náhodné pozice. O tom je entropie: a multiplicita stavů systému musí vždy vzrůst.
Příklady
Které z níže uvedených nastavení je pravděpodobnější je třeba dodržovat uspořádání cihel v průběhu času?

V první konfiguraci je multiplicita stavů bloků je málo: všechny jsou uspořádány v směrhorizontální, paralelní navzájem. S postupem času nebo jednáním agenta se očekává jeho konfigurace
vyrůst v číslo v Státy, zvýhodňující pondělíkonformace, znázorněno na obrázku vpravo. Lze uvést další příklady:-
Když je ledový balíček umístěn do nádoby s většíteplota, jeho teplota stoupá, dokud nedosáhne tepelná bilance. V tomto bodě se led může roztát. Opětovným odebíráním tepla z ledového bloku, který je nyní ve stavu kapalný, může se znovu stát pevným, ale jeho konformací nebude mít stejnou organizaci které byly dříve prezentovány.
Nepřestávejte... Po reklamě je toho víc;)
Když otevřete láhev parfému, může vám pomoci teplo difúze vašeho molekuly, šíření obsahu parfému po celé délce místnosti. Nelze očekávat opak, protože odstranění tepla by nepodporovalo návrat molekul do baňky.
Matematická definice entropie
THE matematická definice entropie je dána poměrem množství tepla (Q) přenášené mezi dvěma částmi tepelně izolovaného systému v joulů (J), svou absolutní teplotou, v Kelvin (K.):

S = Entropie (J / K)
ΔQ = Množství tepla (J)
T = Absolutní teplota (K)
Výše uvedená definice platí pro izotermické procesy, tj. ve kterých dochází k tak malým (nebo pomalým) výměnám tepla, že nejsou schopny změnit teplotu systému. Definice entropie je tedy infinitezimální (nekonečně malá část).
Pojem entropie můžeme také pochopit následovně: být systémem tvořeným dvěma částmi stejného plynu v mnoho různýchteploty, je možné extrahovat určité množství práce o tom, že některé hýbe píst nebo ruční klika, například. Nicméně, přesčas, části tohoto plynu budou mít tendenci Zůstatektepelný. Pokud již nebude teplotní rozdíl, a to ani při přítomnosti veškeré přítomné energie, nebude možné žádnou extrahovat práceužitečný od něho.
Autor: Rafael Hellerbrock
Vystudoval fyziku
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
HELERBROCK, Rafaeli. „Co je to entropie?“; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/o-que-e/fisica/o-que-e-entropia.htm. Zpřístupněno 28. června 2021.


