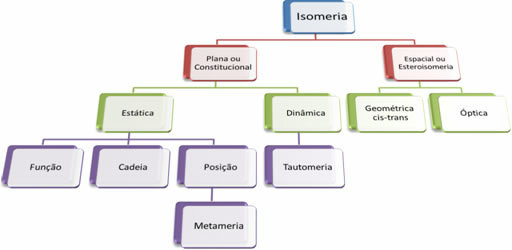
Jelikož existují tisíce organických sloučenin, může mít fenomén izomerismu několik forem. Izomerismus lze tedy v zásadě rozdělit do dvou typů: plochý nebo ústavní izomerismus a vesmírná izomerie nebo stereoizomerie. Každý uvedený typ lze rozdělit, jak ukazuje následující diagram:
Podívejte se na každý případ:
1. Plochý nebo ústavní izomerismus: Izomery tohoto typu mají stejný molekulární vzorec a vyznačují se plochými strukturními vzorci. Existuje pět případů rovinného izomerismu: funkce, řetěz, poloha, metamerismus a tautomerismus.
1.1.Funkční nebo funkční izomerismus: Rozdíl mezi izomery je ve funkční skupině.
Příklad: Molekulární vzorec C3H6Ó
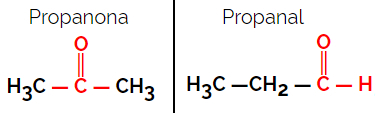
Všimněte si, že propanon je z ketonové skupiny a propanal je z aldehydové skupiny.
1.2. Řetězové nebo kosterní izomery: Rozdíl mezi izomery je v typu řetězce. Například jeden izomer je otevřený řetězec a druhý s uzavřeným řetězcem, nebo jeden s normálním řetězcem a druhý s rozvětveným řetězcem, nebo jeden je homogenní řetězec a druhý je heterogenní řetězec.
Příklad: Molekulární vzorec C4H10
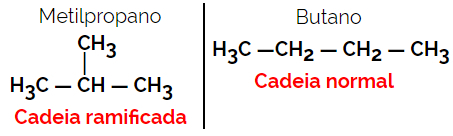
1.3.Poziční nebo poziční izomerismus: Rozdíl je v poloze nenasycenosti, funkční skupiny, heteroatomu nebo substituentu.
Příklad: Molekulární vzorec C4H6

1.4.Kompenzační izomerie nebo metamery: Jedná se o speciální typ izomerismu polohy, kde rozdílem je poloha heteroatomu.
Nepřestávejte... Po reklamě je toho víc;)
Příklad: Molekulární vzorec C4H10Ó
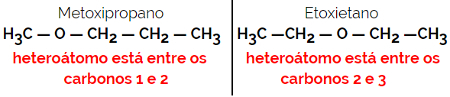
1.5.Dynamická izomerie nebo tautomerie: Jedná se o speciální typ isomerismu funkcí, ve kterém izomery koexistují v dynamické rovnováze v roztoku. Dva hlavní typy tautomerie jsou mezi ketonem a enolem (rovnováha ketoenolu) a mezi aldehydem a enolem (rovnováha aldoenolu).
Příklad: Molekulární vzorec C3H6Ó
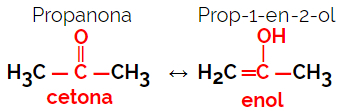
2. Vesmírný izomerismus nebo stereoizomerismus: V tomto případě lze rozdíl mezi izomery zobrazit pouze prostřednictvím orientace jejich atomů v prostoru. Existují dva typy stereoizomerismu: geometrický izomerismus a optický izomerismus.
2.1.Geometrické nebo cis-trans izomery: Rozdíl je v tom, že izomer byl pojmenován jako cis má stejné uhlíkové ligandy v dvojné vazbě nebo v cyklických sloučeninách na stejné straně roviny. Izomerní ligandy trans jsou na opačných stranách.
Příklad: Molekulární vzorec C2H2Cl2

Tyto sloučeniny se nazývají stereoizomery.
2.2.Optický izomer: Nastává, když jsou izomery schopné odchýlit paprsek polarizovaného světla. Pokud ohýbá polarizovaný paprsek světla doleva, jedná se o levotočivý izomer, ale pokud se ohýbá doprava, nazývá se pravostranný izomer.
Příklad:
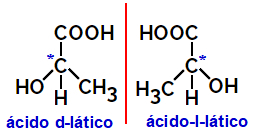
Asymetrické molekuly, jako jsou ty, které jsou uvedeny výše, které jsou vzájemnými zrcadlovými obrazy a které nejsou překrývající se, se nazývají enantiomery.
Autor: Jennifer Fogaça
Vystudoval chemii
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
FOGAÇA, Jennifer Rocha Vargas. „Druhy izomerismu“; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/tipos-isomeria.htm. Zpřístupněno 28. června 2021.
Funkce, pozice, funkce, řetězu, tautomery, řetězu, řetězu, metamery.
Pozice, funkce, řetězu, řetězu, tautomery, řetězu, polohy, metamery.
Z pozice, z řetězu, z řetězu, z řetězu, tautomery, z řetězu, z polohy, tautomery.
Z pozice, z funkce, z řetězce, z funkce, tautomery, z řetězce, z pozice, metamery.

