Organické sloučeniny lze reprezentovat různými způsoby, například plochým strukturním vzorcem, zjednodušeným nebo kondenzovaným strukturním vzorcem nebo pomlčkovým vzorcem. Nejjednodušší reprezentace je však pomocí molekulárního vzorce.

Podívejme se tedy, jak určit molekulární vzorec organických sloučenin na základě ostatních výše uvedených vzorců.
1. Plochým strukturním vzorcem:tento vzorec ukazuje uspořádání nebo uspořádání atomů v molekule. Například níže je plochý strukturní vzorec jednoho z uhlovodíků přítomných v benzínu.

Všimněte si, že v tomto vzorci jsou zobrazeny všechny atomy a všechny existující vazby mezi nimi. Nyní, Chcete-li určit molekulární vzorec této sloučeniny, stačí spočítat počet atomů každého prvku a umístit index na pravou dolní stranu příslušného prvku.
Důležitým aspektem, který je třeba zdůraznit, je to vždy začínáme molekulární vzorec organických sloučenin z prvku uhlík, protože je hlavní složkou těchto látek. Viz příklad:
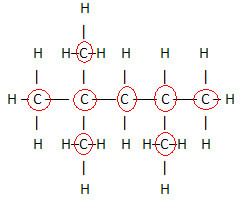
Jelikož existuje 8 atomů uhlíku, začneme psát molekulární vzorec takto: C8
K dokončení tohoto vzorce spočítáme množství vodíku:
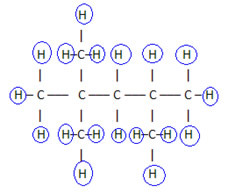
Takže vaše molekulární vzorec é C8H18.
2. Prostřednictvím zjednodušeného nebo zhuštěného strukturního vzorce: v tomto typu vzorce je množství vodíku zkráceno. Podívejte se například na stejný vzorec pro molekulu nacházející se v benzínu, nyní v kondenzované formě:
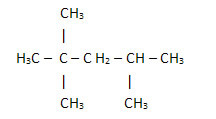
Nepřestávejte... Po reklamě je toho víc;)
Tímto způsobem je ještě snazší spočítat množství vodíků, stačí přidat indexy (3 +3+ 3 +2 +1 +3 +3 = 18).
Nyní se ale podívejme na kondenzovaný strukturní vzorec kyseliny linolové, který existuje v zelenině, jako je bavlna, sója, slunečnice atd. a který se používá v barvách a lacích:
H3C─CH2CH2CH2CH2CH═CH─CH2CH═CH─CH2CH2CH2CH2CH2CH2CH2─COOH
Počítáme-li množství uhlíků, vodíku a kyslíku, máme následující molekulární vzorec kyseliny linolové: C18H32Ó2.
3. Prostřednictvím vzorce tahu: tento vzorec dále zjednodušuje způsob reprezentace organických sloučenin, protože vynechává skupiny C, CH, CH2 a CH3.
Příkladem je linolová molekula, podívejte se, jak vypadá:

Nejprve spočítáme množství uhlíků, pamatujme si, že v tomto vzorci je každá vazba mezi uhlíky představována pomlčkou. Špičky, stejně jako dva inflexní body, tedy odpovídají atomům uhlíku.
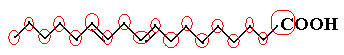
Takže máme: C18
Nyní, abychom spočítali množství vodíků, si musíme pamatovat, že vazby mezi uhlíky a vodíky jsou implikovány, protože je známo, že uhlík vytváří čtyři vazby; tedy množství chybějících vazeb je množství vodíku vázaného k tomuto prvku.
Viz vysvětlení níže:
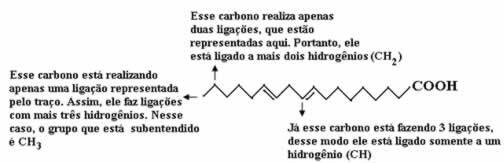
Množství vodíku tedy bude: 32.

Množství kyslíku lze spočítat poměrně snadno, protože jsou pouze dva. Protože molekulární vzorec é: C18H32Ó2.
Autor: Jennifer Fogaça
Vystudoval chemii
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
FOGAÇA, Jennifer Rocha Vargas. "Molekulární vzorce organických sloučenin"; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/formulas-moleculares-compostos-organicos.htm. Zpřístupněno 28. června 2021.
Uhlíkový prostorový vzorec, Lewisův elektronový vzorec, rovinná struktura, elektronické páry, vazba kovalentní, valenční vrstva, vývoj atomového modelu, molekulární vzorec, strukturní vzorec, vzorce trojrozměrný.
Chemické vzorce, plochý strukturní vzorec, Couperův strukturní vzorec, trojná vazba, plyn dusík, elektronový vzorec, Lewisův vzorec, molekulární vzorec, jednoduchá vazba, dvojná vazba, plyn uhličitý.