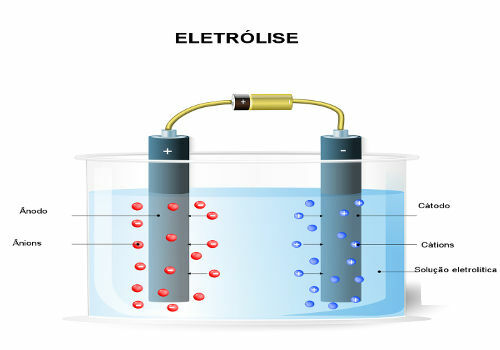
Elektrolýza je proces, který má široké průmyslové uplatnění, a proto jsou jeho kvantitativní aspekty pro továrny nesmírně důležité. Potřebují například vědět, kolik činidla použít, jak dlouho proces provést a kolik požadovaného produktu získá.
Prostřednictvím magné elektrolýzy chloridu sodného (kuchyňská sůl) průmyslová odvětví vyrábějí plynný chlór, takže potřebují vědět, jaké množství plynného chlóru budou moci získat.
Kromě toho několik kovových dílů prochází elektrolýzou ve vodném prostředí, aby bylo možné je potáhnout jiným kovem, jako je tomu v případě zlatých nebo stříbrných polodrahokamů a bižuterie. Kvalita barvy potaženého předmětu a účinnost ochrany proti jeho korozi závisí mimo jiné na době elektrolýzy a intenzitě použitého elektrického proudu.
Anglický fyzik a chemik Michael Faraday (1791-1867) tedy začal tyto aspekty studovat zahrnující elektrolýzu a po několika experimentech objevil některé zákony v tom případě.

Michael Faraday (1791-1867)
Jeden z nich ukázal, že množství hmoty kovu, které je uloženo na elektrodě, je přímo úměrné množství elektrického náboje (Q), který prochází obvodem.
Elektrický náboj (Q) je dán následujícím vzorcem:

O tom, co:
i = intenzita elektrického proudu (jednotka: ampér - A)
t = čas (jednotka: sekundy - s)
Jednotkou nabíjení by tedy byla A. s, což se rovná coulombově jednotce (C).
Nepřestávejte... Po reklamě je toho víc;)

V roce 1909 fyzik Robert Andrews Millikan (1868-1953) zjistil, že elektrický náboj 1 elektronu se rovná 1,602189. 10-19 C.

Robert Andrews Millikan (1868-1953)
Avogadrova konstanta říká, že v 1 molu elektronů je 6,02214. 1023 elektrony. Množství náboje přenášeného průchodem 1 molu elektronů se tedy rovná součinu elektrického náboje každého elektronu množstvím elektronů, které máme v 1 molu, tj.:
1,602189. 10-19 C. 6,02214. 1023 = 96486 C.
Pokud tedy známe množství hmoty (n), které prochází obvodem, vynásobte ji hodnotou právě jsme viděli, že jsme našli elektrický náboj (Q), který bude potřebný k provedení procesu elektrolýzy jestli chceš:

Tato hodnota (96486 C) je známá jako Faradayova konstanta (1F). Pokud je tedy náboj použitý v procesu uveden v faraday, můžeme použít vztahy stanovené pravidly tří a vypočítat množství hmoty, které bude uloženo v elektrolýze.

Přečíst text Aplikace kvantitativních aspektů elektrolýzy přesně vědět, jak mohou tyto výpočty přispět k řešení problémů souvisejících s procesy elektrolýzy a dokonce i baterií.
Autor: Jennifer Fogaça
Vystudoval chemii
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
FOGAÇA, Jennifer Rocha Vargas. „Kvantitativní aspekty elektrolýzy“; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/aspectos-quantitativos-eletrolise.htm. Zpřístupněno 28. června 2021.
Chemie

Aplikace elektrolýzy, galvanického pokovování, niklování, chromování, niklu, chrómu, katody, sodíku, hliníku, chloru, hydroxid sodný, plynný vodík, magnátní elektrolýza, vodná elektrolýza, alkalické kovy, kovy alkalických zemin, plyn chlór.
Chemie
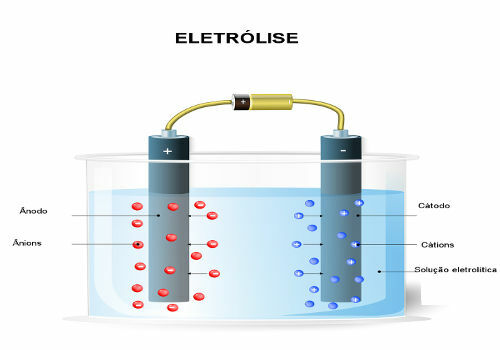
Elektrolýza, roztoky elektrolytů, elektrický proud, oxidačně-redukční reakce, spontánní chemický proces, chemický proces spontánní, transformátor, umělá transformace, průmyslová odvětví, alkalické kovy, alkalické zeminy, plynný vodík, plyn tř