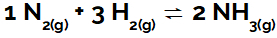أنت غازات هم انهم سوائل والتي ، على عكس السوائل ، تشغل كل المساحة المتاحة للحاوية حيث تكون محصورة. الجزيئات المكونة للغازات حرة في الحركة والتفاعل مع بعضها البعض ومع جدران الحاوية.
ال قانون بويليحدد أن العلاقة بين الضغط وحجم الغاز متناسبة عكسيًا. كلما زاد الضغط على الجزيئات ، قلت المساحة التي تشغلها.
ال قانون جاي لوساكيحدد أن العلاقة بين حجم ودرجة حرارة الغاز تتناسب طرديًا. كلما ارتفعت درجة حرارة الغاز ، زاد اهتياج الجزيئات ، والتي تميل إلى التحرك بعيدًا ، مما يزيد من المساحة التي تشغلها.
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
قانون تشارلز يحدد أن العلاقة بين ضغط ودرجة حرارة الغاز تتناسب طرديًا. كلما ارتفعت درجة حرارة الغاز ، زاد التحريض الجزيئي. وبالتالي ، يزداد معدل حدوث التصادمات بين الجزيئات وجدران الحاوية ، مما يجعل ضغط الغاز أكبر.
ال معادلة كلابيرون يجمع القوانين الثلاثة المذكورة أعلاه ويحدد علاقة واحدة بين متغيرات الدولة.
تي = درجة حرارة الغاز (ك).
لا تنتج الطبيعة غازات لها خصائص الغاز المثالي. الغاز المثالي هو نموذج نظري ومفيد لفهم سلوك الغازات في مواجهة التغيرات في خصائصها.
هل ترغب في الإشارة إلى هذا النص في مدرسة أو عمل أكاديمي؟ نظرة:
جونيور ، جواب سيلاس دا سيلفا. "ما هو الغاز المثالي؟" ؛ مدرسة البرازيل. متوفر في: https://brasilescola.uol.com.br/o-que-e/fisica/o-que-e-gas-perfeito.htm. تم الوصول إليه في 28 يونيو 2021.
ما هي الغازات ، ما هي خواص الغازات ، المركبات الجزيئية ، الانضغاطية ، الحجم الثابت ، الطاقة الحركية يعني ، درجة حرارة مطلقة للغاز ، غاز مثالي ، غازات حقيقية ، غاز كامل ، متغيرات حالة الغاز ، حجم غاز ، مواسم