في أميدات هي مركبات عضوية تتميز ب وجود أ نيتروجين (N) متصلة مباشرة بالكربونيل (C = O). هذه المواد متوفرة بشكل طبيعي ، إحداها موجودة في إفرازات الثدييات (اليوريا) ، ولكن يمكن أيضًا الحصول عليها عن طريق التوليف الاصطناعي.
يمكن إنتاج الأميدات ، على سبيل المثال ، بواسطة تجفيف ملح الأمونيوم، العملية المستخدمة في تصنيع البوليمرات. يتم استخدامها أيضًا كـ اسمدة، نظرا لتوافره من النيتروجين وكيف المخدرات ، لها عمل مضاد للميكروبات.
اقرأ أكثر:أكريلاميد - أميد يمكن أن ينشأ من تسخين بعض الأطعمة
أميد الهيكل
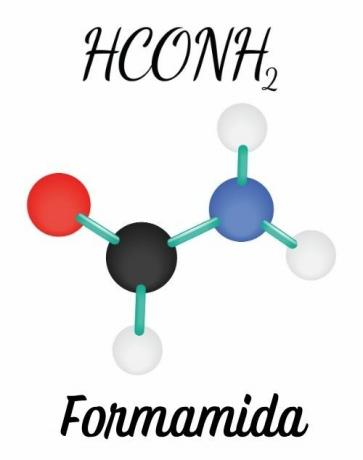
تتشكل الأميدات بواسطة أ نيتروجين مرتبط مباشرة بمجموعة كربونيل أو أسيل (RC = O). الرابطة المزدوجة بين كربون انها ال الأكسجين وإمكانية انتقال هذا الزوج إلى نيتروجين يعطي الجزيء الهندسة المستوية، على عكس الأمينات ، التي لها هندسة هرمية.
تصنيف الأميدات
التصنيف حسب عدد البدائل العضوية
وكذلك الأمينات، يتم تصنيف الأميدات وفقًا لـ عدد الجذور العضوية التي يحل محلها النيتروجينومع ذلك ، بالنسبة للأميدات ، علينا أن نأخذ في الاعتبار أن أحد روابط المجموعة سيكون بالضرورة مجموعة الأسيل ، أي أنه سيكون لدينا فقط أميدات من النوع:
- أميد غير مستبدل: النيتروجين مرتبط باثنين الهيدروجين ومجموعة كاربونيل.
مثال:

- أمين أحادي الاستبدال: يحتوي على نيتروجين مرتبط بهيدروجين ومجموعة كربونيل وجذر عضوي. في هذه الحالة ، حيث تم استبدال أحد الهيدروجين بسلسلة كربون ، ضع في اعتبارك R كمجموعة عضوية.
مثال:

- الأمين المنحل: يحتوي على نيتروجين مرتبط بجذرين عضويين وكربونيل. في هذه الحالة ، تم استبدال الهيدروجين بسلاسل كربون.
مثال:

نرى أيضا: كيفية تصنيف الهاليدات العضوية؟
التصنيف حسب عدد الكاربونيل المرتبطة بالنيتروجين
يمكن أيضًا تصنيف الأميدات وفقًا لعدد الكاربونيل المرتبطة مباشرة بالنيتروجين في الجزيء.
- الأميدات الأولية: مجموعة أسيل واحدة فقط مرتبطة بالنيتروجين (R-CO) NH2 .
- الأميدات الثانوية: مجموعتان من الكربونيل أو الأسيل مرتبطة بالنيتروجين (R-CO)2نيو هامبشاير.
- الأميدات الثلاثية: ثلاث مجموعات أسيل مرتبطة بالنيتروجين (R-CO)3لا.

تسمية الأميدات
ال تسمية الأميدات سيتم تقديمها بواسطة:
بادئة تشير إلى عدد الكربون في السلسلة + الموقع واللون الذي يشير إلى عدم التشبع (إن وجد) + إنهاء أميد |
انظر الجدول أدناه:
بادئة (رقم من الكربون) |
إنفكس (تشبع السلسلة) |
لاحقة (مجموعة وظيفية) |
|||
1 كربون |
التقى- |
مكالمات فردية فقط |
-ان- |
أميدات |
-الأميد |
2 ذرة كربون |
إلخ- |
||||
3 ذرات كربون |
دعم- |
1 رابطة مزدوجة |
-ن- |
||
4 كربون |
لكن- |
||||
5 كربون |
مكبوت- |
2 روابط مزدوجة |
-دين- |
||
6 ذرات كربون |
عرافة- |
||||
7 ذرات كربون |
سبت- |
1 رابطة ثلاثية |
-في- |
||
8 ذرات كربون |
أكتوبر- |
||||
9 ذرات كربون |
عدم- |
2 روابط ثلاثية |
-داخل- |
||
10 ذرات كربون |
ديسمبر- |
يجب أن يبدأ عدد الكربون بالجانب الأقرب لنيتروجين المجموعة الوظيفية.
أمثلة:
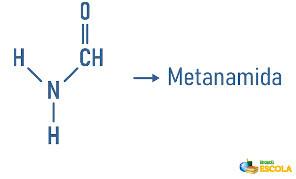



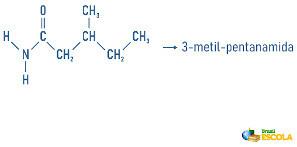
قد تتلقى الأمينات أيضًا في تسمياتها مواصفات لتصنيف الجزيء:
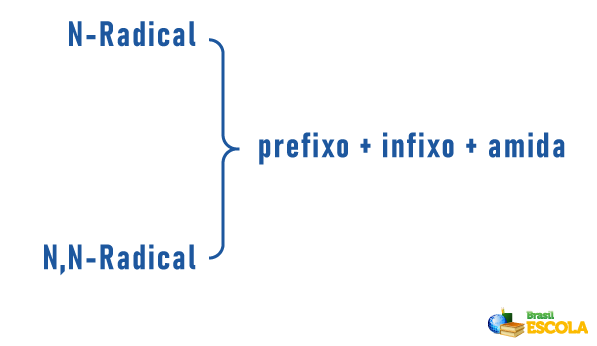
تذكر أن تسمية الراديكاليين تتكون من: صمرجع يشير إلى عدد ذرات الكربون + الإنهاء "il" أو "ila". يتم وضع الراديكاليين في التسمية بالترتيب الأبجدي.
أمثلة:


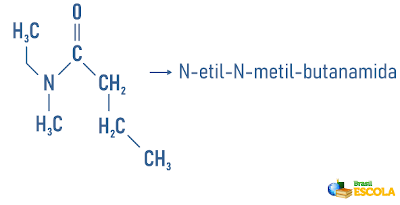
الوصول أيضًا إلى: تسمية الهيدروكربونات الحلقية والمتفرعة
خصائص الأميدات
- نقطة انصهار وغليان عالية ، والتي سيكون لها قيمة متدرجة وفقًا للحجم والترتيب المكاني لسلسلة الكربون.
- عالية القطبية بسبب وجود الكربونيل والنيتروجين.
- رابطة هيدروجين الأميدات الأحادية غير المستبدلة والمستبدلة.
- الجزيئات الأصغر والأبسط قابلة للذوبان في الماء. يتداخل حجم الجزيء أيضًا مع قابلية ذوبان الأميدات: فكلما كانت سلسلة الكربون أكبر ، قلت قابلية الذوبان في الماء.
- للأميدات صفة أساسية بسبب ميلها لاستقبال أيونات H+.
تطبيق الأميدات
- تستخدم كوسطاء في صناعة البولي إيثيلين مثل النايلون.
- تطبق في صياغة العقاقير مثل السلفانيلاميد والبنسلين ، المبادئ الفعالة للأدوية المبيدة للجراثيم للسيطرة على العدوى.
- اليوريا ، التي يمكن الحصول عليها صناعيا أو كمنتج تفرزه الثدييات ، هي مادة من مجموعة الأميد ، ثنائي الأميد. يتم استخدامه كمكمل غذائي في الزراعة وكأسمدة.

الحصول على الأميدات
يمكن العثور على الأميدات بسهولة في شكل طبيعي ، لكن شكلها الاصطناعي لا يزال يستخدم على نطاق واسع في العمليات الصناعية. فيما يلي بعض تفاعلات إنتاج الأميد بناءً على المركبات النيتروجينية الأخرى.
تفاعل تجفيف ملح الأمونيوم

تفاعل الأمينات مع كلوريد الحمض
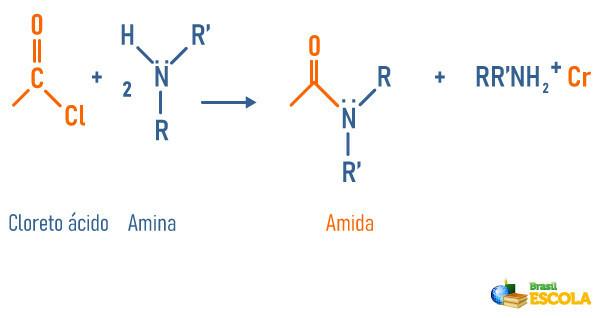
-
تفاعل الأنهيدريدات مع الأمينات
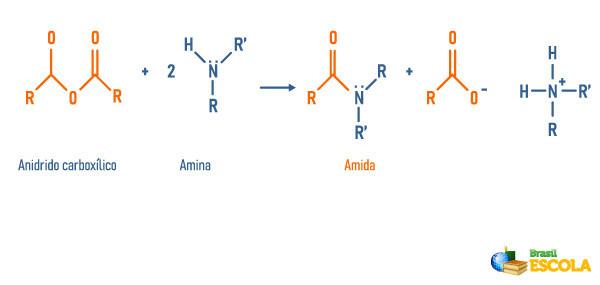
تفاعل الإسترات مع الأمينات

إعادة الترتيب الهيكلي للألدوكسيم
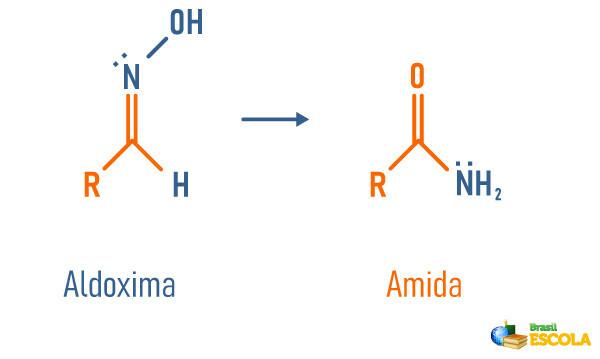
-
ترطيب النتريل
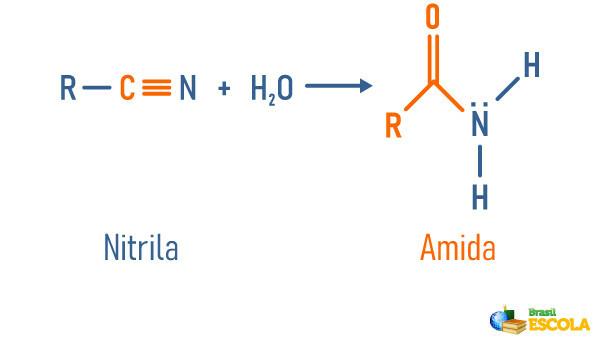
اقرأ أيضا: أميد التحلل المائي - تفاعل يستخدم للحصول على مواد مهمة
تمارين حلها
السؤال رقم 1 - (UFRS) الأسبارتام ، في الصورة أدناه ، هو مُحلي صناعي يستخدم في العديد من المشروبات الغازية والأطعمة منخفضة السعرات الحرارية.

المجموعة المؤطرة في الشكل هي سمة من سمات الوظيفة العضوية
أ) استر.
ب) أميد.
ج) الأحماض الأمينية.
د) أمين.
ه) الكربوهيدرات.
القرار
البديل ب. المجموعة الوظيفية المحددة في الشكل هي أميد ، بسبب وجود الكربونيل (C = O) المرتبط مباشرة بالنيتروجين (N).
السؤال 2 - (UNESP) في أغسطس 2005 ، تم الإبلاغ عن ضبط دفعات من الليدوكائين كان من الممكن أن تسبب وفاة العديد من الأشخاص في البرازيل ، بسبب مشاكل التصنيع. هذا الدواء هو مخدر موضعي يستخدم على نطاق واسع في فحوصات التنظير الداخلي ، مما يقلل من إزعاج المريض. هيكلها الجزيئي موضح أدناه:
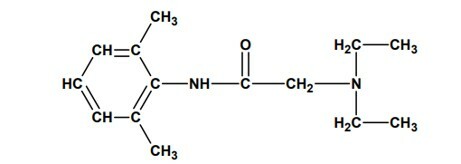
ويعرض الوظائف:
أ) أمين ثانوي وأمين ثالث.
ب) أميد وأمين ثالثي.
ج) الاميد والاستر.
د) الإستر والأمين العالي.
هـ) الإستر والأمين الثانوي.
القرار
البديل ب.
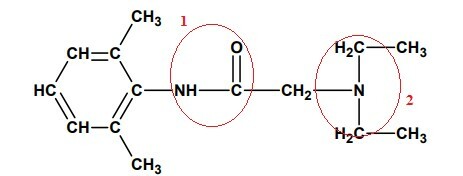
بعد تحديد وترقيم الأجزاء المميزة لكل دالة عضوية ، دعنا نحلل كل منها:
1- هي AMIDA لوجود مجموعة الأسيل (R-C = O) مرتبطة مباشرة بالنيتروجين ، أحادي الاستبدال.
2- حيث لا يوجد لدينا مجموعة الأسيل (R-C = O) ، ولكن فقط النيتروجين المرتبط مباشرة بالكربون الآخر في هذه المجموعة لدينا أمين ثلاثي ، لأن جميع الهيدروجين الثلاثة ، المرتبط سابقًا بالنيتروجين ، قد تم استبداله بمجموعات عضوي.
بقلم Laysa Bernardes Marques de Araújo
مدرس كيمياء


