الأحماض الكربوكسيلية هي مركبات عضوية تحتوي على مجموعة وظيفية كربوكسيل ، أي الكربون الذي يصنع رابطة مزدوجة مع الأكسجين ورابطة واحدة مع مجموعة OH.
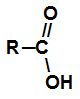
الكربوكسيل هو المجموعة الوظيفية لكل حمض كربوكسيلي
على المدى حمض الكربوكسيل يستخدم لتعيين وظيفة عضوية مؤكسجة ، أي وظيفة تحتوي على ذرة أكسجين في بنيتها. المركبات التي تنتمي إلى هذه المجموعة لها قدرة تآكل وطعم حامض ، لأنها حمضية.
خصائص الأحماض الكربوكسيلية
بشكل عام ، فهي قابلة للذوبان في المذيبات العضوية ؛
الأحماض الكربوكسيلية الوحيدة القابلة للذوبان في الماء هي تلك التي تحتوي على ما يصل إلى أربع ذرات كربون في بنيتها ؛
بشكل عام ، تكون الأحماض الكربوكسيلية أكثر كثافة من الماء ، باستثناء الأحماض التي تحتوي على ذرة كربون واحدة أو اثنتين ؛
الأحماض الكربوكسيلية التي تحتوي على ما يصل إلى تسعة ذرات كربون سائلة في درجة حرارة الغرفة ؛
في الحالة الصلبة ، تكون بيضاء ولها مظهر شمعي ؛
في الحالة السائلة ، تكون عديمة اللون.
نظرًا لأن لديهم الكربوكسيل ، فإنهم قادرون على التأسيس روابط هيدروجينية;
مركباتها قطبية.
بشكل عام ، تكون عديمة الرائحة ، باستثناء الأحماض التي تحتوي على ما يصل إلى ثلاثة ذرات كربون ذات رائحة مزعجة ، وتلك التي تحتوي على ما يصل إلى ستة ذرات كربون لها رائحة مقززة ؛
حكم تسمية الأحماض الكربوكسيلية
لأداء تسمية من حمض الكربوكسيليحدد الاتحاد الدولي للكيمياء البحتة والتطبيقية (IUPAC) القاعدة التالية:
حامض
+
بادئة (تشير إلى عدد الكربون في السلسلة)
+
infix (يشير إلى نوع الروابط بين ذرات الكربون)
+
مرحبا شارك
انظر بعض الأمثلة:
حمض الكربوكسيل مع ست ذرات كربون
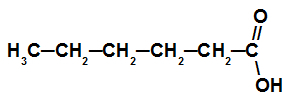
يحتوي هذا الحمض على سلسلة من ست ذرات كربون (بادئة سداسية عشرية) ، وروابط مفردة فقط (إنفكس آن) وكربوكسيل (أويك) ، لذا فإن اسمه هو حمض سداسي.
حمض الكربوكسيل مع سبع ذرات كربون
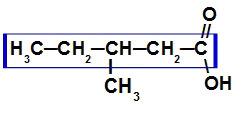
نظرًا لأن هذا الحمض متفرّع ، فإن السلسلة الرئيسية هي التي تحتوي على أكبر عدد من الكربون والكربوكسيل. في هذا المركب ، تحتوي السلسلة الرئيسية على خمس ذرات كربون (بادئة مكبوتة) ، روابط مفردة فقط بين ذرات الكربون (infix an) و carboxyl (oic) ، لذلك اسمها حمض 3-ميثيل بنتانويك.
ملاحظة: يجب أن يبدأ ترقيم السلسلة الرئيسية دائمًا من الكربون الكربوكسيل.
حمض الكربوكسيل مع اثنين من الكربوكسيل
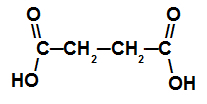
يحتوي هذا الحمض على سلسلة بها أربع ذرات كربون (بادئة ولكن) ، روابط مفردة فقط بين ذرات الكربون (infix an) واثنين من ذرات الكربوكسيل (dioic) ، ومن هنا اسمها حمض حمض البوتانيديك.
ملاحظة: بين infix و "dioic" ، تمت إضافة حرف علة متصل.
التفاعلات الكيميائية مع الأحماض الكربوكسيلية
ال) تفاعل الأسترة
إنه تفاعل كيميائي يتفاعل فيه حمض الكربوكسيل مع أ كحول وشكل واحد استر والماء كما هو موضح في المعادلة التالية:

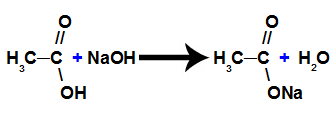
ب) رد فعل التمليح
إنه تفاعل كيميائي يتفاعل فيه حمض الكربوكسيل مع قاعدة غير عضوية ويشكل ملحًا من حمض الكربوكسيل والماء ، كما هو موضح في المعادلة التالية:
ç) رد فعل القضاء
في هذا التفاعل ، يتم تجفيف جزيئين من حمض الكربوكسيل ، مما يؤدي إلى أ أنهيدريد والماء كما هو موضح في المعادلة التالية:

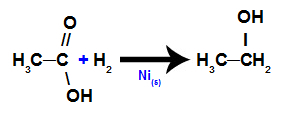
د) الحد من الأحماض الكربوكسيلية
في هذا التفاعل ، يتعرض حمض الكربوكسيل لوسط يحتوي على غاز الهيدروجين (H2) والنيكل الصلب ، مما يؤدي إلى تكوين الكحول ، كما هو موضح في المعادلة التالية:
تطبيقات الأحماض الكربوكسيلية
إنتاج الإسترات العضوية.
إنتاج أملاح حمض الكربوكسيل ؛
تحضير العطور
إنتاج الخل
إنتاج الحرير الصناعي.
إنتاج المطهرات
صباغة الأقمشة.
بي ديوغو لوبيز دياس
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-acidos-carboxilicos.htm
