دراسات الكيمياء مهمة والتحولات التي تمر بها. المادة ، بدورها ، هي كل ما يشغل حيزًا في الفضاء ، وبالتالي ، له كتلة وحجم. يمكن العثور عليها بطريقتين أساسيتين: مواد و مخاليط.
كما هو موضح في النص "ما هي المادة؟"، يتم تكوين المادة عندما يتم تكوين مادة معينة بواسطة نوع واحد فقط من المكونات (والتي يمكن أن تكون جزيئات مثل الذرات والجزيئات ، معادلات الوحدات ، الإلكترونات أو الأيونات) ونتيجة لذلك ، لها خصائص فيزيائية مثل نقطة الانصهار ، نقطة الغليان والكثافة ، ثابتة وجيدة. معرف.
سابقا المخاليط عبارة عن أنظمة مكونة من مركبين أو أكثر أو مواد بسيطة مختلفة. بهذه الطريقة ، فإنها تقدم خصائص فيزيائية غير محددة ومتغيرة. تعتمد هذه الخصائص على كمية كل مادة في الخليط وطبيعتها.
الخريطة الذهنية: الخلطات
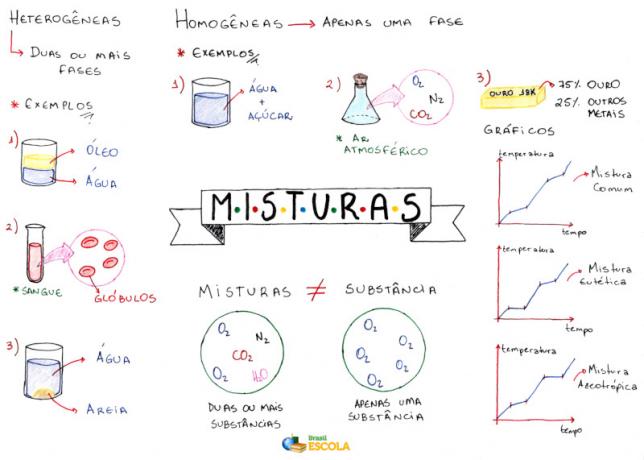
* لتنزيل الخريطة الذهنية بصيغة PDF ، انقر هنا!
على سبيل المثال ، الكحول الإيثيلي الشائع الذي نستخدمه للتنظيف والتطهير ليس مادة نقية ، لأنه لا يتكون فقط من جزيئات الإيثانول (H3C-CH2-أوه). كما يشير الملصق الموجود على زجاجة هذا المنتج ، فهو خليط من الإيثانول والماء (H2س). على سبيل المثال ، إذا رأيت على الملصق أن الكحول يحتوي على تركيز 96 ميكروجرام (درجات جاي-لوساك) ، فهذا يعني أنه في 100 جزء من هذا الخليط ، هناك 96 جزءًا من الإيثانول و 4 أجزاء من الماء ، أي أن زجاجة 100 مل من الكحول المائي تحتوي على 96 مل من الإيثانول و 4 مل من ماء.
يمكن تصنيف المخاليط إلى متجانس و غير متجانسة. في حالة الكحول المائي ، لدينا خليط متجانس. لكن ما هو الخليط المتجانس؟ إنه خليط لا يمكننا فيه رؤية فصل مكوناته. كامل طوله منتظم وله طور واحد.
تسمى هذه المخاليط المتجانسة أيضًا حلول، مع وجود جزيئات مشتتة بقطر أصغر من 1 نانومتر ، أي أنه حتى مع وجود مجهر فائق الدقة ، يمكن رؤية أكثر من مرحلة واحدة في هذه المواد. علاوة على ذلك ، لا يمكن فصل مكوناته بالطرق الفيزيائية مثل أجهزة الطرد المركزي أو الترشيح.
الدم خليط. بالعين المجردة ، يبدو أنه خليط متجانس ، لكنه ليس كذلك ، لأننا نرى مكوناته تحت المجهر. علاوة على ذلك ، عند وضعها في جهاز طرد مركزي ، يتم فصل هذه المكونات.

الدم المطرود من المركز وصورته تحت المجهر
يمكن أن تكون المخاليط أو المحاليل المتجانسة في جميع الحالات الفيزيائية الثلاث. يعتبر الكحول المائي المذكور مثالاً على خليط سائل. الهواء هو خليط الغاز يتكون من عدة غازات ، أهمها النيتروجين (N2) والأكسجين (O2). السبائك المعدنية مخاليط صلبة، مثل الصلب الذي يتكون من حوالي 98.5٪ حديد (حديد) ، 0.5 إلى 1.7٪ C (كربون) وآثار من Si (السيليكون) ، S (كبريت) و P (فوسفور).
في مخاليط غير متجانسة، من ناحية أخرى، هي تلك التي لديها أكثر من مرحلة واحدة، مثل خلط الماء والزيت والماء والرمل والجرانيت (خليط من الكوارتز والميكا والفلسبار) وما إلى ذلك.

مثال على خليط غير متجانس من ثلاث مراحل
كما ذكرنا ، فإن الخصائص الفيزيائية للخلائط ليست ثابتة ولا محددة. ومع ذلك ، هناك بعض المخاليط التي تعتبر استثناءات ، المخاليط الأزيوتروبي و سهل الانصهار. تحتوي المخاليط الأزيوتروبية على نقطة غليان أو تكثيف ثابتة ، وتتصرف ، في هذه المرحلة ، كمادة نقية.. 96٪ كحول المذكور عبارة عن خليط أزيوتروبي لأنه يحتوي على نقطة غليان ثابتة عند 78.2 درجة مئوية.
الآن نعم، المخاليط سهلة الانصهار هي تلك التي تتصرف كما لو كانت مادة نقية فقط أثناء التصلب أو نقطة الانصهار. ومن الأمثلة على ذلك السبيكة المعدنية المصنوعة من 40٪ كادميوم و 60٪ بزموث ، ولها نقطة انصهار ثابتة تساوي 140 درجة مئوية.
لكن الغالبية العظمى من المخاليط تغير حالتها الفيزيائية ليس عند درجة حرارة ثابتة ، ولكن عند نطاقات درجة حرارة غير محددة.
الخريطة الذهنية بقلم الأم فيكتور ريكاردو فيريرا
مدرس كيمياء
بقلم جينيفر فوغاسا
تخرج في الكيمياء
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-uma-mistura.htm