غازمثالي هو واحد حيث الاصطدامات بين الجسيمات مرنة تمامًا. بين جسيماته ، لا يوجد أي نوع من التفاعل ، مثل القوات جذابة أو مثيرة للاشمئزاز ، علاوة على ذلك ، فإن هذه الجسيمات لا تشغل حيزًا.
وفقا ل النظرية الحركية للغازات، الحالة الديناميكية الحرارية للغاز المثالي موصوفة بالكامل بواسطة متغيرات الضغطوالحجم و درجة الحرارة.
نظرةأيضا: قياس السعرات الحرارية: الخريطة الذهنية والصيغ والتمارين التي تم حلها
مفهوم الغاز المثالي
تتكون الغازات المثالية حصريًا من حبيباتفيأبعادمنضبط (بحجم ضئيل) الموجودة في حركةفوضوية قيد التشغيل عالي● السرعة. في هذا النوع من الغاز ، تكون درجة الحرارة وسرعة ترجمة الجزيئات متناسبة.
نظرًا لعدم وجود تفاعل بين جزيئات الغاز المثالي ، فإن الطاقة الداخلية من هذا الغاز دائمًا يساوي مجموع الطاقة الحركية من كل الجسيمات التي تتكون منه.
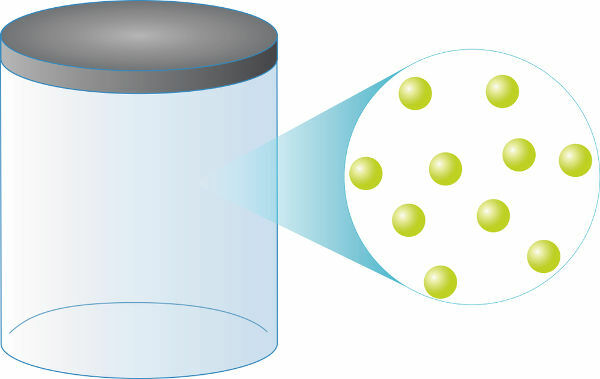
مهما كانت الغازات المثالية ، فستظل دائمًا متشابهة عددفيحبيبات لنفس الحجم. كتلتها ، بدورها ، سوف تعتمد مباشرة على الخاص بك الكتلة المولية (يقاس بالجرام / مول) ، بالإضافة إلى ذلك ، 1 مول من الغاز المثالي (حوالي 6.0.1023 الجزيئات) ستشغل دائمًا أ حجم يساوي 22.4 لتر.
أنت غازاتحقيقة، حيث يوجد حدوث الاصطداماتغير مرن بين الجسيمات ، يقترب جدًا من سلوك الغازات المثالية في أنظمة الضغط المنخفض ودرجات الحرارة المرتفعة. من قبيل الصدفة ، في ظل الظروف العادية للضغط ودرجة الحرارة على الأرض (25 درجة مئوية و 1 ضغط جوي) ، فإن معظم تتصرف الغازات مثل الغازات المثالية ، وهذا يسهل حساب التنبؤات حول السلوك الديناميكي الحراري هم.
بعض الغازات ، مثل بخار الماء، وهو مخفف في غاز الغلاف الجويلايمكن اعتبارها غازات مثالية بل نعم غازاتحقيقة. هذه الغازات لها تفاعلات كبيرة بين جزيئاتها ، والتي يمكن تكثف، مما تسبب لهم سائل إذا كان هناك واحد انخفاض درجة الحرارة.
خصائص الغازات المثالية
تحقق من ذلك في نبذة مختصرةبعض خصائص الغازات المثالية:
- في نفوسهم تحدث فقط تصادمات مرنة تمامًا بين الجسيمات ؛
- في نفوسهم لا توجد تفاعلات بين الجسيمات.
- فيها الجسيمات لها أبعاد ضئيلة ؛
- 1 مول من الغاز المثالي يشغل حجم 22.4 لترًا ، بغض النظر عن ماهية الغاز ؛
- تتصرف الغازات الحقيقية مثل الغازات المثالية عندما تكون تحت ضغط منخفض وأنظمة درجات حرارة عالية ؛
- تتصرف معظم الغازات بشكل مشابه للغازات المثالية.
قانون الغاز المثالي
دراسة الغازات التي طورها العلماء تشارلزبويلجوزيفلويسمثلي الجنس لوساك و روبرتبويل أدى إلى ظهور ثلاثة قوانين تجريبية، تستخدم لشرح سلوك الغازات المثالية في أنظمة درجة الحرارة, الضغط و أربعة حجمالخامسالثوابت على التوالى.
شكلت هذه القوانين معًا الأساس الضروري لظهور قانون الغاز المثالي، والتي تتعلق ب الحالة الديناميكية الحرارية الأولية للغاز، التي تحددها الكميات P.1، ت1 و V.1، مع الخاص بك الحالة الديناميكية الحرارية النهائية (ص2، الخامس2 و ت2) ، بعد أن عانى البعض تحويل الغاز.
تفحص ال معادلة من قانون الغاز العام:
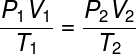
ينص قانون الغاز العام على أن منتج يعطي الضغط الفراء أربعة حجمالخامسمنغاز، مقسومًا على درجة الحرارة الديناميكية الحرارية ، بوحدة كلفن ، يساوي ثابتًا. هذا الثابت ، بدوره ، موصوف بواسطة معادلة كلابيرون، يشاهد:
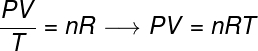
لا - عدد الشامات (مول)
ص - الثابت العام للغازات الكاملة (0.082 atm.l / mol. كلفن أو 8.31 جول / مول. ك)
في الصيغة ، ص هو الضغط الذي يمارسه الغاز ، الخامس هو الحجم الذي يشغله هذا الغاز ، و تي هي درجة الحرارة مقاسة بوحدة كلفن. عظمة لا يشير إلى عدد الشامات ، بينما ص هو الثابت العالمي للغازات المثالية ، والذي يقاس غالبًا بوحدات atm.l / mol. ك أو في J / مول. K ، هذا الأخير يتم اعتماده من قبل SI.
نظرةأيضا:ما هي الرياح الشمسية وكيف تؤثر على الغلاف الجوي للأرض؟
الطاقة الداخلية للغاز المثالي
ال طاقةداخلي من الغازات المثالية يمكن حسابها باستخدام المنتج بين ثابتفيبولتزمان ودرجة الحرارة الديناميكية الحرارية ، لاحظ:
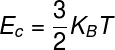
كب - ثابت بولتزمان (كب = 1,38.10-23 ي / ك)
من العلاقة السابقة التي تسمح لنا بحساب متوسط الطاقة الحركية من جزيئات الغاز المثالي ، نرسم الصيغة التالية ، والتي يمكن استخدامها لحساب ماهية يعني السرعة المربعة للجزيئات من غاز مثالي ، لدرجة حرارة معينة T ، لاحظ:
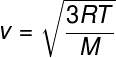
م - الكتلة المولية (جم / مول)
تسمح لك هذه الصيغة برؤية ملف إضافةفيدرجة الحرارة للغاز المثالي يؤدي إلى زيادة في متوسط السرعة التربيعية للجسيمات.
تعرف أكثر:اكتشف ما هو الضوء وما هي خصائصه
تمارين محلولة على الغازات المثالية
السؤال رقم 1) تم العثور على مولين من الغاز المثالي ، عند ضغط 1 ضغط جوي ، عند درجة حرارة 227 درجة مئوية. احسب باللتر الحجم الذي يشغله هذا الغاز.
البيانات: R = 0.082 atm.l / mol. ك
أ) 75 لتر
ب) 82 لتر
ج) 15 لتر
د) 27 لتر
ه) 25 لتر
قالب: حرف الباء
القرار:
لحساب حجم هذا الغاز ، سنستخدم معادلة كلابيرون ، ومع ذلك ، قبل إجراء الحساب ، من الضروري تحويل درجة حرارة 227 درجة مئوية إلى كلفن. لهذا نضيف العامل 273 إلى درجة الحرارة هذه ، مما ينتج عنه درجة حرارة 500 كلفن.
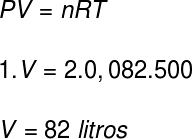
وفقًا للقرار ، يبلغ الحجم الذي يشغله الغاز 82 لترًا.
السؤال 2) يحتل الغاز المثالي حجمًا 20 لترًا ، عندما يتعرض لضغط 3 ضغط جوي ، بحيث تظل درجة حرارته ثابتة ، بينما يتضاعف حجمه ثلاث مرات. احسب الضغط النهائي لهذا الغاز بعد أن يمر بهذا التحول.
أ) 1 أجهزة الصراف الآلي
ب) 3 أجهزة الصراف الآلي
ج) 5 أجهزة الصراف الآلي
د) 8 أجهزة الصراف الآلي
ه) 9 أجهزة الصراف الآلي
قالب: الحرف ا
القرار:
لحل هذا التمرين ، سنستخدم القانون العام للغازات ، لاحظ:
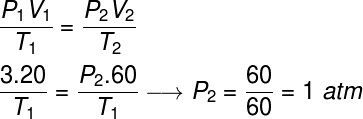
لإجراء الحساب ، كان من الضروري تخصيص حجم 60 لترًا للغاز ، حيث تضاعف حجمه ثلاث مرات أثناء التحويل.
بقلم رافائيل هيلربروك
مدرس الفيزياء
