ملح رطب إنها ملح حيث تدمج أيونات المركب جزيئات الماء في شبكاتها البلورية ، مما يجعل هذه الجزيئات جزءًا من بلورة الملح.
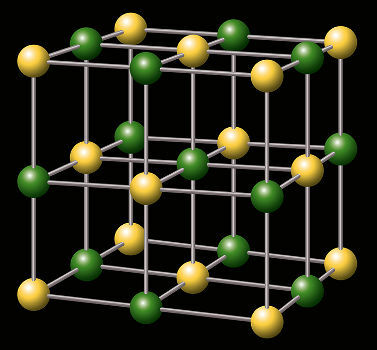
تمثيل شعرية بلورية من الملح
الصيغة الكيميائية لل ملح رطب يتبع نمطًا يكون لدينا فيه وجود أي كاتيون (X+) ، أي أنيون (Y-) وكمية معينة (ن) في مولات الماء ، كما يتضح في النموذج التالي:
XY.nH2ا
لتشكيل تسمية من ملح رطبيجب علينا تنفيذ القواعد التالية:
اسم أنيون + دي + اسم الكاتيون + بادئة + رطب
ملحوظة: البادئة المشار إليها في قاعدة التسمية تشير إلى الكمية في مول من الماء الموجودة في صيغة الملح ، وبالتالي ، لـ 1 مول (أحادي) ، 2 مول (د) ، 3 مول (ثلاثي) ، إلخ.
المثال الأول: FeCl2.2 ح2ا
يحتوي هذا الملح المائي على المكونات التالية:
كاتيون الحديد الثاني (Fe+2);
أنيون كلوريد (Cl-);
2 مولات من H.2O (بادئة دي).
لذلك سيكون اسمها ثنائي كلوريد الحديد الثاني.
المثال الثاني: MgSO447.H2ا
يحتوي هذا الملح المائي على المكونات التالية:
المغنيسيوم كاتيون (ملغ+2);
أنيون كبريتات (SO4-2);
7 مول من H.2O (بادئة هيبتا).
لذلك سيكون اسمها هو كبريتات المغنيسيوم هيبتاهيدراتي.
المثال الثالث: ZnBr28.H2ا
يحتوي هذا الملح المائي على المكونات التالية:
كاتيون الزنك (Zn+2);
أنيون البروميد (Br-1);
8 مول من H.2O (بادئة ثماني).
لذلك سيكون اسمها ثماني الهيدرات بروميد الزنك.
تعديل كيميائي
عندما يخضع الملح المائي لعملية تسخين ، يتم إطلاق جزيئات الماء المدمجة في التركيب البلوري في شكل بخار ، تاركًا ملحًا بسيطًا فقط.
بي ديوغو لوبيز
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-sal-hidratado.htm