في تحول متساوي الحرارة ، فإن اختلاف الحجم والضغط من غاز معين ، ولكن درجة حرارة ثابتة; ومن هنا أصل الاسم متساوي الحرارة (اليوناني: ايزو = يساوي ؛ ثيرمو = الحرارة).
أجرى العالمان Boyle و Mariotte ، بشكل منفصل ، تجارب مماثلة وكانت النتيجة التي تم الحصول عليها: مع زيادة الضغط ، ينخفض حجم الغاز.
فقط فكر ، على سبيل المثال ، في مكبس حقنة. إذا طبقنا ضغطًا خارجيًا على هذا المكبس ، أي إذا قمنا بزيادة الضغط ، سينخفض حجم الهواء المشغول داخل المحقنة ، والعكس صحيح.
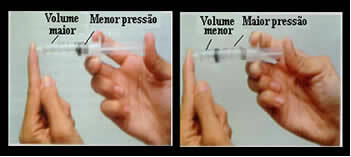
الحجم والضغط متناسبان عكسيًا: في اللوحة اليسرى ، يكون الضغط صغيرًا والحجم الذي يشغله الهواء كبير. على اليمين ، عندما يتم تطبيق المزيد من الضغط على مكبس المحاقن ، ينخفض الحجم.
هذه ليست حالة معزولة ، إنها شيء يتكرر بانتظام مع الغازات. لذلك تم ذكر هذه الحقيقة في شكل قانون يمكن وصفه على النحو التالي:
| قانون بويل أو قانون بويل ماريوت: تحت درجة حرارة ثابتة ، يتناسب الحجم الذي تشغله كتلة ثابتة من الغاز عكسًا مع ضغطه. |
هذا يعني أننا إذا ضاعفنا ضغط الغاز ، فإن حجمه سينخفض إلى النصف وهكذا. عندما تكون كميتان من هذه الكميات متناسبة عكسيًا ، يكون ناتجهما ثابتًا ؛ وهكذا ، رياضياً ، يمكن تمثيل هذه العلاقة على النحو التالي:
| PV = ك |
حيث k = ثابت.
وبالتالي ، إذا كانت لدينا في الحالة الأولى قيمة ضغط غاز معين مثل P1 وحجمه على أنه V1 ، فعلينا أن:
| ص1. الخامس1 = ك |
إذا قمنا بزيادة هذا الضغط إلى P2 ، فسيتم تغيير حجمه أيضًا إلى V2 ومرة أخرى سيتعين علينا:
| ص2 . الخامس2 = ك |
وهكذا نصل إلى الاستنتاج:
| ص1. الخامس1 = ص2. الخامس2 |
يمكن رؤية هذا الثبات من خلال المثال الوارد في الجدول أدناه ، لضغوط وأحجام الغاز بكتلة ثابتة:
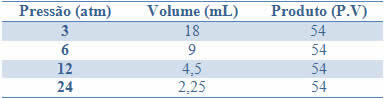
من خلال رسم هذه القيم ، سنرى تشكيل منحنى.
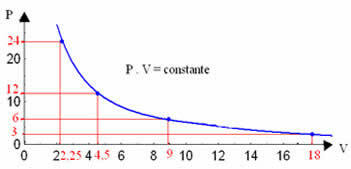
سيكون التمثيل الرسومي للتحول متساوي الحرارة دائمًا قطعًا زائدًا ، بغض النظر عن قيم الضغط والحجم ودرجة الحرارة التي أجريت بها التجربة. يسمى هذا القطع الزائد متساوي الحرارة; لذلك ، كما يتضح من الرسم البياني أدناه ، تؤدي درجات الحرارة المختلفة إلى تساوي درجة حرارة مختلفة.
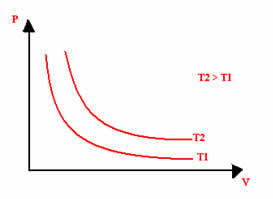
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/quimica/transformacao-isotermica-ou-lei-boyle.htm

