تهجين هو الاسم الذي يطلق على اندماج أو اتحاد المدارات الذرية غير المكتملة ، وهي ظاهرة تزيد من عدد روابط تساهمية يمكن أن تفعله الذرة. تذكر أن المدار هو منطقة الذرة حيث يوجد احتمال أكبر لإيجاد إلكترون.
معرفة عدد الروابط التي تصنعها الذرة وفهم ظاهرة تهجينمن الضروري معرفة بعض النقاط الأساسية حول الذرة:
1ا النقطة: المستويات الفرعية للطاقة
المستويات الفرعية للطاقة التي يمكن أن تمتلكها الذرة هي s و p و d و f.
2ا النقطة: عدد المدارات لكل مستوى فرعي
يحتوي كل مستوى فرعي للطاقة على كمية مختلفة من المدارات ، كما نرى أدناه:
المستوى الفرعي: 1 مداري ؛
ع المستوى الفرعي: 3 مدارات ؛
المستوى الفرعي د: 5 مدارات.
يتم التمثيل العام لهذه المدارات على النحو التالي:
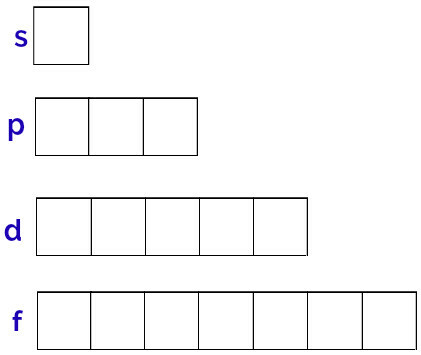
تمثيل مدارات كل مستوى فرعي
وفقًا لباولي ، يمكن أن يحتوي المدار على إلكترونين كحد أقصى ، مع يدور (حركات الدوران) عكس ذلك.
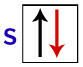
تمثيل المدار s بإلكتروناته
وفقًا لهوند ، لا يتلقى مدار مستوى فرعي الإلكترون الثاني إلا عندما تكون جميع المدارات الأخرى من هذا المستوى الفرعي قد تلقت بالفعل الإلكترون الأول.
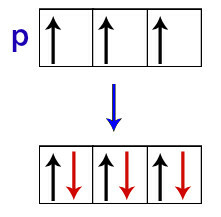
توزيع الإلكترونات في مدارات المستوى الفرعي p
3ا النقطة: التوزيع الإلكتروني
لفهم التهجين وعدد الروابط التي تصنعها الذرة ، من الضروري تنفيذ التوزيع الإلكتروني على مخطط لينوس بولينج.

مخطط لينوس بولينج
تذكر أن الحد الأقصى لعدد الإلكترونات في كل مستوى فرعي هو:
ق = 2 إلكترون ؛
ع = 6 إلكترونات ؛
د = 10 إلكترونات ؛
f = 14 إلكترونًا.
بعد هذا الاستعراض الموجز ، يمكننا تحديده الآن ما هو التهجين. لهذا ، سوف نستخدم عنصر البورون الكيميائي (العدد الذري = 5) كمثال.
عندما نقوم بالتوزيع الإلكتروني للبورون ، يكون لدينا:
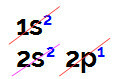
توزيع البورون الإلكتروني في مخطط لينوس بولينج
من الممكن أن نلاحظ في هذا التوزيع أن البورون يحتوي على إلكترونين في المستوى الفرعي s وإلكترون واحد في المستوى الفرعي p من طبقة التكافؤ.
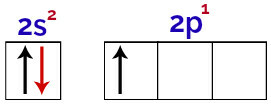
الإلكترونات في مدارات طبقة تكافؤ البورون
نظرًا لأن البورون له مدار واحد غير مكتمل ، فإنه يجب أن يصنع رابطة تساهمية واحدة فقط ، لأن عدد الروابط دائمًا ما يرتبط ارتباطًا مباشرًا بعدد المدارات غير المكتملة.
وهكذا ، عندما تستقبل ذرة البورون الطاقة من البيئة الخارجية ، تصبح إلكتروناتها ، خاصة تلك الموجودة في غلاف التكافؤ ، متحمسة. يؤدي هذا إلى مغادرة أحد الإلكترونات من المدار s واحتلال أحد المدارات p الفارغة ، مما ينتج عنه 3 مدارات ذرية غير كاملة ، كما ترون في الصورة التالية:

تمثيل الحالة المثارة لذرة البورون
أخيرًا ، هناك اتحاد المدار s غير المكتمل مع المدارات p غير المكتملة. هذا الاتحاد يسمى تهجين. نظرًا لأن لدينا اندماج المدار s مع اثنين p ، فإنه يطلق عليه تهجين ص2.
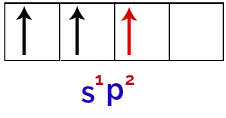
تمثيل المدارات المهجنة في ذرة البورون
بالإضافة إلى البورون ، تخضع العديد من العناصر الكيميائية الأخرى لظاهرة التهجين ، مثل الكبريت (S) ، والزينون (Xe) ، الفوسفور (ف) ، كربون (ج) ، البريليوم (يكون).
بي ديوغو لوبيز دياس
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-hibridizacao.htm
