يتم الحصول على الألمنيوم من خلال العمليات المعدنية. علم المعادن هو مجال يدرس تحول الخامات إلى معادن أو سبائك معدنية. يتم الحصول على العديد من المعادن بهذه الطريقة ، مثل النحاس والتيتانيوم والحديد والمنغنيز.
في حالة الألومنيوم ، يكون الخام الرئيسي المستخدم هو البوكسيت (الشكل) الذي يحتوي على أكسيد الألومنيوم المميأ (Aℓ2ا3. س ح2س) وشوائب مختلفة.

في تعدين الألمنيوم ، تحدث الخطوات الأربع التالية:
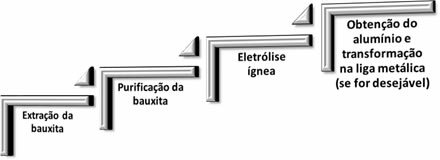
عندما يكون أكسيد الألومنيوم (Aℓ2ا3 (ق)) عن البوكسيت ، يصبح اسمه الألومينا.
في السابق ، كان يتم عمل ما يلي: تمت معالجة الألومينا بحمض الهيدروكلوريك لتوليد كلوريد الألومنيوم ؛ التي تم وضعها للتفاعل مع البوتاسيوم المعدني أو الصوديوم ، مما يؤدي إلى اختزال المركب وظهور الألمنيوم المعدني:
أ2ا3 (ق) + 6 HCℓ(هنا)→ 4 AℓCℓ3 (عبد القدير) + 3 ح2ا(ℓ)
ACℓ3 (عبد القدير) + 3 ك(س)→ 3 KC(س) + أ(س)
ومع ذلك ، كانت هذه الطريقة باهظة الثمن وغير فعالة ، لذلك كان الألمنيوم يعتبر معدنًا نادرًا.
ولكن في عام 1886 ، طور عالمان بشكل منفصل الطريقة المذكورة أعلاه ، والتي تم فيها استخدام التحليل الكهربائي البركاني. هؤلاء العلماء هم الأمريكي تشارلز م. هول والفرنسي بول هيرولت ، لهذا سميت هذه الطريقة
عملية هول هيرولت أو ببساطة،عملية القاعة، في حين أن تشارلز م. حصل على براءة اختراع هول.كانت النقطة الأساسية التي اكتشفوها هي كيفية صنع سائل أكسيد الألومنيوم للقيام بذلك. تكون قادرة على أداء التحليل الكهربائي البركاني ، حيث كانت المشكلة أن نقطة انصهارها كانت أعلى 2000 درجة مئوية. استخدموا خام كريوليت متدفق (Na3AℓF6) ، والذي كان قادرًا على خفض درجة حرارة انصهار أكسيد الألومنيوم إلى حوالي 1000 درجة مئوية.
وهكذا ، كما هو مبين في الرسم البياني أدناه ، تم وضع هذا الخليط من أكسيد الألومنيوم والكريوليت في وعاء التحليل الكهربائي المصنوع من الصلب المبطن بالكربون. يمر تيار كهربائي عبر هذا الخليط المصهور. تعمل جدران الحاوية التي تلامس الخليط كقطب سالب للتحليل الكهربائي (الكاثود) ، حيث يحدث اختزال كاتيونات الألومنيوم. الأنود (القطب الموجب) عبارة عن أسطوانات مصنوعة من الجرافيت أو الكربون ، أي كلاهما مصنوع من الكربون ، حيث يحدث أكسدة أنيون الأكسجين:
تفاعل نصف الكاثود: 4 Aℓ3+(ℓ) + 12 و- → 4 أℓ(ℓ)
تفاعل نصف الأنود: 6 س2-(ℓ) → 12 و- + 3 س2 (ز)
يتفاعل الأكسجين المتكون مع الكربون الموجود في الأنود ويولد أيضًا ثاني أكسيد الكربون:
3 س2 (ز) + 3 ج(س) → 3 كو2 (ز)
لذا فإن التفاعل العام والمخطط لهذا التحليل الكهربائي البركاني الذي يؤدي إلى ظهور الألمنيوم يتم إعطاؤه من خلال:

يكون الألمنيوم الذي تم الحصول عليه في صورة سائلة ، لأن درجة انصهاره تبلغ 660.37 درجة مئوية ، أي أقل من درجة انصهار خليط الألومينا والكريوليت. الألومنيوم أيضًا أكثر كثافة من الخليط ، وبالتالي ، يتم ترسيبه في قاع الحاوية ، حيث يتم تجميعه.
في إنتاج 1 طن من الألمنيوم يتم استخدامه:
- من 4 إلى 5 أطنان من البوكسيت، من أين 2 طن من الألومينا;
- 50 كجم من الكريوليت (لا توجد الكثير من الاحتياطيات الطبيعية من الكريوليت ، لذلك يتم الحصول عليها عادةً من خلال تركيبها من الفلوريت (CaF2) ، وهو معدن وفير في الطبيعة) ؛
- 0.6 طن من الفحم للأقطاب الكهربائية.
يتجاوز إنتاج الألومنيوم سنويا 27.4 مليون طن.
من بين سبائك الألمنيوم الرئيسية لدينا ما يلي:

بقلم جينيفر فوغاسا
تخرج في الكيمياء
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/quimica/obtencao-aluminio-por-meio-eletrolise.htm

