العنصر الكيميائي الفوسفور (P) ينتمي إلى الفترة الثالثة من الجدول الدوري وعائلة النيتروجين (VA). لهذا السبب ، تتكون ذراتها عادة من ثلاث ذرات روابط كيميائية للوصول إلى نظرية الثماني (المزيد). ومع ذلك ، هناك بعض المواقف التي تصنع فيها ذرة الفوسفور أكثر من ثلاث روابط ، وهي حقيقة لا يمكن تحقيقها إلا من خلال ظاهرة التهجين.
لفهم تهجين الفوسفور ، يجب أن نفهم أولاً سبب تكوين ذرة هذا العنصر لثلاثة روابط. للقيام بذلك ، نحتاج فقط إلى مراقبة التوزيع الإلكتروني الخاص بك:

توزيع الفوسفور الإلكتروني
يمكننا أن نلاحظ أنه في طبقة التكافؤ ، تحتوي ذرة الفوسفور على المستوى الفرعي 3s الكامل (مع إلكترونين) والمستوى الفرعي 3p غير المكتمل (كل من المدارات الثلاثة ذات المستوى الفرعي p لها إلكترون). أدناه لدينا توزيع الإلكترونات في مدارات المستويات الفرعية لـ طبقة التكافؤ الفوسفور:
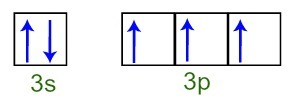
تمثيل إلكترونات غلاف التكافؤ لذرة الفوسفور
نظرًا لأن كل من المدارات ذات المستوى الفرعي 3p غير مكتملة ، فإن ذرة الفوسفور قادرة على تكوين ثلاث روابط كيميائية ، وبالتالي تحقيق الاستقرار.
الآن عندما ننظر إلى مادة PCl5، على سبيل المثال ، نحن على يقين من أن الفوسفور في هذا الجزيء قد خضع لعملية تهجين ، حيث قام بخمسة وصلات. نظرًا لأن الكلور ، الذي ينتمي إلى عائلة VIIA ، يحتاج إلى رابطة ليكون مستقرًا والجزيء يحتوي على خمس ذرات من هذا عنصر ، كل منهم يجب أن يصنع رابطة ، مما يجعل ذرة الفوسفور ، بدورها ، يجب أن تصنع خمسة روابط. هذا التواجد ممكن فقط من خلال
تهجين (اتحاد مدارات ذرية غير مكتملة) من الفوسفور.عند تلقي الطاقة من البيئة الخارجية ، تصبح إلكترونات ذرة الفوسفور متحمسة. بعد فترة وجيزة ، ينتقل أحد الإلكترونين المنتمين إلى المستوى الفرعي 3s إلى مدار فارغ موجود في المستوى الفرعي d ، والذي حتى ذلك الحين لا يحتوي على أي إلكترونات. انظر الرسم البياني أدناه:
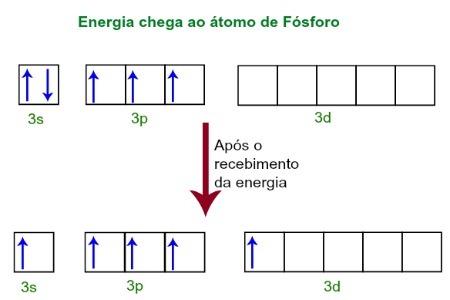
عند تلقي الطاقة ، يتم إثارة إلكترونات الفوسفور ويحتل المرء مدارًا من المستوى الفرعي d.
في هذه اللحظة ، لدينا في طبقة التكافؤ للفوسفور مداري s وثلاثة مدارات p ومدار d غير مكتمل.في النهاية ، تهجين هذه المدارات الخمسة ، أي تندمج ، مما ينتج عنه خمسة مدارات ذرية غير كاملة ، والتي أصبحت الآن قادرة على تكوين خمس روابط كيميائية.

تهجين المدارات الذرية غير المكتملة للفوسفور
كمدار s ، تم ربط ثلاثة مدارات p ومدار d ، يكون تهجين الفوسفور من النوع ص3د.
بي ديوغو لوبيز دياس
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/quimica/hibridizacao-fosforo.htm
