محلول منظم إنه خليط متجانس لا يغير الأس الهيدروجيني أو الأس الهيدروجيني عند إضافة كميات صغيرة من حمض قوي أو قاعدة قوية إلى هذا الخليط. ومع ذلك ، فإن الخليط لا يغير الأس الهيدروجيني أو الأس الهيدروجيني إلا إذا قدم أحد التركيبتين أدناه:
سدادة حامض (الرقم الهيدروجيني أقل من 7):
يحتوي على حمض ضعيف ممزوج بـ ملح قابل للذوبان له نفس الأنيون ، مثل حمض الهيدروسيانيك (HCN) وسيانيد البوتاسيوم (KCN) ، والتي لها نفس أنيون السيانيد (CN).
المخزن المؤقت الأساسي (الرقم الهيدروجيني أكبر من 7):
يتمركز مختلطًا ضعيفًا مع ملح له نفس الكاتيون ، مثل هيدروكسيد الزنك [Zn (OH)2] وكلوريد الزنك (ZnCl2) ، والتي لها نفس كاتيون الزنك (Zn+2).
من المهم ، لفهم تأثير المحلول المنظم على تلقي حمض أو قاعدة قوية ، أن نتذكر متى تعتبر الأحماض والقواعد قوية:
→ ترتيب القواعد من حيث القوة
قوي: قواعد تحتوي على عناصر كيميائية من عائلات IA (الفلزات القلوية) و IIA (معادن الأرض القلوية) ، باستثناء المغنيسيوم ؛
ضعيف: القواعد التي تحتوي على عنصر المغنيسيوم وآخر ، طالما أنها لا تنتمي إلى عائلات IA و IIA.
→ تصنيف حمض للقوة
أ) بالنسبة للهيدرات (الأحماض الخالية من الأكسجين):
قوي: HCl و HBr و HI فقط ؛
المعتدلين: HF فقط ؛
ضعيف: أي هيدروكسيد آخر.
ب) بالنسبة للأكسجين (الأحماض مع الأكسجين):
قوي: عندما يكون طرح عدد الأكسجين بواسطة عدد الهيدروجين مساويًا أو أكبر من 2 ؛
المعتدلين: عندما يكون طرح عدد الأكسجين بعدد الهيدروجين يساوي 1 ؛
ضعيف: عندما يكون طرح عدد الأكسجين بواسطة عدد الهيدروجين مساويًا أو أقل من 0.
تأثير إضافة قاعدة قوية إلى المخزن المؤقت
للتوضيح ، دعنا نستخدم الامتداد محلول منظم يتكون من هيدروكسيد الزنك [Zn (OH)2] والملح القابل للذوبان من كلوريد الزنك (ZnCl2) ، والتي ستتلقى كمية صغيرة من قاعدة هيدروكسيد الصوديوم القوية (NaOH). انظر الأرصدة الموجودة في هذا المحلول المؤقت:
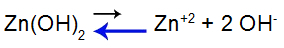
معادلة توازن تفكك القاعدة
يتحول التوازن إلى اليسار لأن القاعدة ضعيفة.
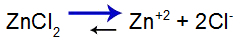
معادلة توازن تفكك الملح
يتحول الميزان إلى اليمين لأن الملح قابل للذوبان.
القاعدة القوية لديها التوازن التالي:
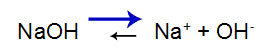
معادلة توازن تفكك القاعدة
يتحول التوازن إلى اليمين لأن القاعدة قوية.
تطلق القاعدة القوية المضافة أنيون الهيدروكسيد (OH) في الماء-) ، التي لها قابلية عالية لكاتيونات الزنك (Zn+2) من الملح في التوازن الثاني. الارتباط بين الهيدروكسيد والزنك يشكل هيدروكسيد الزنك:
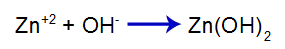
معادلة تكوين القاعدة
لذا فإن OH- من القاعدة يقلل من كمية الزنك في التوازن الثاني ويزيد من كمية القاعدة [Zn (OH)2] ، مما يؤدي إلى مزيد من الانفصال وإطلاق كاتيونات الزنك+2 في التوازن الأول. نظرًا لأننا لن يكون لدينا تغيير في كمية الهيدروكسيد في الوسط ، لذلك لا يتغير الرقم الهيدروجيني.
تأثير إضافة حمض قوي إلى المخزن المؤقت
للتوضيح ، دعنا نستخدم المحلول الذي يتكون من هيدروكسيد الزنك [Zn (OH)2] وبواسطة ملح كلوريد الزنك القابل للذوبان (ZnCl2) ، والتي ستتلقى كمية صغيرة من حمض الهيدروديك (HI) ، وهو قوي. انظر الأرصدة الموجودة في الغطاء:
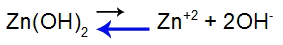
معادلة توازن تفكك القاعدة
تحول التوازن إلى اليسار لأن القاعدة ضعيفة.
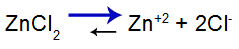
معادلة توازن الملح
تحول التوازن إلى اليمين لأن الملح قابل للذوبان.
يحتوي الحمض القوي على التوازن التالي:
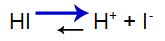
معادلة التوازن الحمضي
تحول التوازن إلى اليمين لأن الحمض قوي.
ينتج الحمض المضاف كاتيون الهيدرونيوم في الماء (H+) ، التي لها صلة عالية بأيونات الهيدروكسيد (OH-) من القاعدة. يشكل الارتباط بين الهيدرونيوم والهيدروكسيد جزيء ماء:
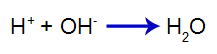
معادلة تكوين الماء
لذا فإن H+ من الحمض يقلل من كمية الهيدروكسيدات في التوازن الأول ، مما يزيد من تفكك القاعدة. نظرًا لأننا لن يكون لدينا تغيير في كمية الهيدروكسيد في الوسط ، لذلك لا يتغير الرقم الهيدروجيني.
بي ديوغو لوبيز دياس
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-uma-solucao-tampao.htm

