يمثل الرقم الهيدروجيني الجهد الأيوني للهيدروجين و pOH هو الجهد الأيوني الهيدروكسي للحلول.
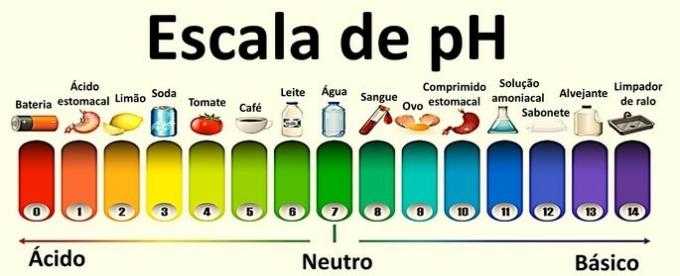
هذه هي المقاييس اللوغاريتمية المستخدمة لقياس الطابع الحمضي والأساسي للعينة.
تتراوح القيم التي تتكون منها من 0 إلى 14 وتم الحصول عليها من التوازن الأيوني للماء.
يحتوي المحلول المحايد على درجة حموضة 7. القيم أقل من 7 تصنف الحلول على أنها حمضية ، بينما بعد 7 الحلول أساسية.
باستخدام قيمة الأس الهيدروجيني ، من الممكن إيجاد القيمة المقابلة على مقياس الأس الهيدروجيني ، فقط عن طريق إجراء عملية طرح.
توازن الماء الأيوني
جزيء الماء لديه القدرة على التأين وفقًا للمعادلة:
هنا لدينا توازن أيوني ، لأن العملية قابلة للانعكاس ويمكن للأيونات أيضًا أن تتجمع وتشكل جزيء ماء مرة أخرى.
هناك طريقة أخرى لإثبات التوازن الذي يحدث من خلال التأين الذاتي.
ينتج جزيء الماء أيونات الهيدرونيوم (H3ا+) والهيدروكسيل (OH-) من خلال تعطيل الجزيء الثاني.
المنتج الأيوني للماء (K.ث)
ثابت التوازن الأيوني للماء هو:
نظرًا لأن الماء سائل نقي ، فإن تركيزه يؤخذ على أنه 1 ولا يتعارض مع القيمة الثابتة. لذلك ، يصبح التعبير:
ا المنتج الأيوني لـ ماء é .
هذا التعبير يتلقى الرمز K.ث (W يأتي من الكلمة الإنجليزية ماء - ماء) ومثله مثل ثابت التوازن ، يختلف باختلاف درجة الحرارة.

تحديد الأس الهيدروجيني والأس الهيدروجيني
عند درجة حرارة 25 درجة مئوية ، يكون المنتج الأيوني للماء:
في تأين الماء النقي ، 1 مول من H3ا+ يتكون من 1 مول من OH- .
هكذا،
نظرًا لأن هذه القيم منخفضة للغاية ، فقد تقرر استخدام قيم كولوغاريتمات ، والتي تتوافق مع اللوغاريتم بعلامة مبادلة.
عند تطبيق الكولوغاريتم على المنتج الأيوني للماء ، علينا:
يمكننا ملاحظة ما يلي: إذا عرفنا الرقم الهيدروجيني لمحلول ما ، فيمكن إيجاد قيمة الأس الهيدروجيني عن طريق طرح القيمة الأولى من 14.
حموضة وأساسيات الحلول
حل محايد: تركيز أيونات الهيدرونيوم يساوي تركيز الهيدروكسيل.
| [H3ا+] = 1,0. 10-7 مول / لتر | الرقم الهيدروجيني = 7 |
| [أوه-] = 1,0. 10-7 مول / لتر | pOH = 7 |
مثال: ماء نقي.
محلول حامض: تركيز أيونات الهيدرونيوم أكبر من تركيز الهيدروكسيل.
| [H3ا+] |
الرقم الهيدروجيني |
| [أوه-] |
pOH |
مثال: الصودا والليمون والطماطم.
الحل الأساسي: تركيز الهيدروكسيل أكبر من تركيز أيونات الهيدرونيوم.
| [H3ا+] |
الرقم الهيدروجيني |
| [أوه-] |
pOH |
مثال: بيض وصابون ومبيض.
حساب الأس الهيدروجيني
تم إنشاء مفهوم الإمكانات الهيدروجينية بواسطة الكيميائي الدنماركي Peter Lauritz Sorensen (1868-1939) للتعبير عن حموضة المحلول من خلال تركيز H+.
انظر الجدول أدناه الذي يوضح تأين a حامض:
| المولارية الأولية | 0,020 | 0 | 0 |
| التأين | 0,001 | 0,001 | 0,001 |
| مولارية في التوازن | 0,019 | 0,001 | 0,001 |
في المثال لدينا أن تركيز H أيونات+ é 0,001. لذلك ، فإن الرقم الهيدروجيني للمحلول هو:
[H+] = 0,001 = 10-3
الرقم الهيدروجيني = - سجل 10-3 = 3
نظرًا لأن الرقم الهيدروجيني للمحلول أقل من 7 ، فإن هذا المحلول حمضي.
ملخص عن الأس الهيدروجيني والأس الهيدروجيني
| تعريفات | الرقم الهيدروجيني: الجهد الأيوني الهيدروجين للمحلول. | |
|---|---|---|
| pOH: الإمكانات الهيدروكسيلية للمحلول. | ||
| الصيغة العامة | الرقم الهيدروجيني + الرقم الهيدروجيني = 14 | |
| حلول | حيادي | الرقم الهيدروجيني = الرقم الهيدروجيني = 7 |
| حمضي |
الرقم الهيدروجيني pOH> 7 |
|
| الأساسيات |
pOH الرقم الهيدروجيني> 7 |
|
| حساب الأس الهيدروجيني | الرقم الهيدروجيني = - سجل [H.+] | |
| حساب الأس الهيدروجيني | pOH = -log [OH-] |
تمارين على الأس الهيدروجيني والأس الهيدروجيني
1. (FMTM) الرقم الهيدروجيني لعصير المعدة ، محلول مائي من حمض الهيدروكلوريك (HCℓ) ، هو حوالي 2. لذلك ، فإن الكتلة ، بالجرام ، من HCℓ الموجودة في كل لتر من عصير المعدة هي
البيانات: الكتل المولية (جم / مول) H = 1 ، Cℓ = 35.5
أ) 7.3 · 10-2
ب) 3.65 10-1
ج) 10-2
د) 2
هـ) 10
البديل الصحيح: ب) 3.65 · 10-1.
الخطوة الأولى: احسب تركيز أيونات الهيدروجين+.
الخطوة الثانية: احسب الكتلة المولية لـ HCl.
الخطوة الثالثة: احسب كتلة حمض الهيدروكلوريك في كل لتر من عصير المعدة.
2. (UEMG) العديد من منتجات التنظيف تحتوي على الأمونيا في تكوينها. يشير ملصق أحد هذه المنتجات إلى أن الرقم الهيدروجيني = 11. هذا يعني أن تركيز كاتيونات الهيدروكسون وأنيونات الهيدروكسيل في هذا المنتج هي على التوالي:
إلى 1. 10-3 و 1. 10-11
ب) 1. 10-11 و 1. 10-7
ج) 1. 10-11 و 1. 10-3
د) 1. 10-11 و 1. 10-11
البديل الصحيح: ج) 1. 10-11 و 1. 10-3.
من الخطأ. تتوافق هذه التركيزات مع محلول pH = 3.
ب) خطأ. على الرغم من أن تركيز H+ تشير إلى أن الرقم الهيدروجيني للمحلول هو 11 ، تركيز أيونات OH- خطأ ، حيث يجب أن يكون 3 ، لأن: pOH = 14 - pH.
ج) صحيح. الرقم الهيدروجيني = 11 و pOH = 3 ، حيث أن الرقم الهيدروجيني + الأس الهيدروجيني = 14.
د) خطأ. على الرغم من أن تركيز H+ تشير إلى أن الرقم الهيدروجيني للمحلول هو 11 ، تركيز أيونات OH- خطأ ، حيث يجب أن يكون 3 ، لأن: pOH = 14 - pH.
أ) 0.1 مول / لتر هيدروكسيد الصوديوم
ب) كلوريد الصوديوم 0.5 مول / لتر
ج) ح2فقط4 1.0 مول / لتر
د) 1.0 مول / لتر حمض الهيدروكلوريك
ه) 0.2 مول / لتر KOH
البديل الصحيح: هـ) KOH 0.2 مول / لتر.
من الخطأ. الحل أساسي لأن الرقم الهيدروجيني الخاص به أكبر من 7 ، لكنه لا يحتوي على درجة حموضة أعلى للبدائل.
ب) خطأ. كلوريد الصوديوم هو ملح لأنه نتاج تفاعل قوي مع حمض وقاعدية. لذلك ، فإن درجة الحموضة فيها محايدة.
ج) خطأ. حمض الكبريتيك هو حمض قوي ، لذلك فإن درجة الحموضة فيه منخفضة.
د) خطأ. حمض الهيدروكلوريك هو حمض قوي ، لذلك فإن درجة الحموضة فيه منخفضة.
ه) صحيح. الحل أساسي لأن الأس الهيدروجيني أكبر من 7.