رد الفعل القابل للانعكاس الذي يكون في حالة توازن لن يتغير توازنه إلا إذا كان هناك أي تغيير خارجي ، لأن التوازن لا يتغير أبدًا من تلقاء نفسه.
أحد هذه التغييرات هو اختلاف التركيز ، والذي يتضمن إزالة أو إضافة الكواشف أو المنتجات.
لنلقي نظرة على مثال:
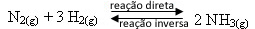
- إضافة الكواشف:
إذا أضفنا المزيد من غاز الهيدروجين أو المزيد من غاز النيتروجين إلى التوازن ، فإن تركيزات المواد المتفاعلة ستزداد ، وبالتالي عدد ستزداد أيضًا الصدمات الفعالة بين جزيئاتها ، مما يؤدي إلى زيادة معدل تطور تفاعل تكوين الأمونيا المباشر. (NH3 (ز)).
هذا يعني أن إضافة الكواشف يغير التوازن إلى الجانب الأيمن ، نحو تكوين المنتجات:

هذا يتوافق مع مبدأ Le Chatelier الذي يقول ذلك عندما يحدث بعض الاضطراب في نظام في حالة توازن ، فإنه يتحرك في اتجاه إلغاء هذا الاضطراب ، في محاولة للتكيف مع توازن جديد.
في الحالة أعلاه ، سيحدث أنه بمرور الوقت ستزداد كمية الأمونيا لتصل إلى التوازن مرة أخرى. وبالتالي ، فإن النسبة بين تركيزات المنتجات والكواشف ستبقى ثابتة ، أي أن قيمة ثابت التوازن Kc ستبقى كما هي.
كك = __ [نيو هامبشاير3]2__↑
[ن2]. [ح2]3 ↑
سيحدث هذا أيضًا في الحالات الأخرى ، أي لن يؤدي أي اختلاف في تركيز الكواشف أو المنتجات إلى تغيير قيمة Kc.
- إضافة المنتجات:
إذا أضفنا المزيد من الأمونيا ، وزيادة تركيزها ، سيتحول جزء منها إلى غازات النيتروجين والهيدروجين ، مما يزيد من معدل تطور التفاعل العكسي لتشكيل الكواشف.
هذا يعني أن إضافة المنتجات يغير الميزان إلى اليسار ، نحو تكوين الكواشف:
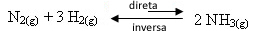
- إزالة الكواشف:
إذا أزلنا أحد الكواشف أو كليهما ، فإن تركيزاتهما ستنخفض ، وبالتالي ، سينخفض معدل تطور التفاعل المباشر. وبالتالي ، سيتم تحويل التوازن نحو تكوين المزيد من المواد المتفاعلة ، إلى اليسار:
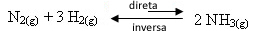
- سحب المنتج:
إذا قللنا تركيز المنتجات ، سينخفض معدل التفاعل العكسي ، مما يزيد من معدل تطور التفاعل الأمامي. هذا يعني أن الميزان سيتحول إلى اليمين:
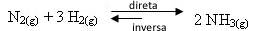
باختصار يمكننا أن نقول ما يلي:

من المهم التأكيد على أن التباين في تركيز المواد الصلبة لا يغير التوازن.
لذلك ، في التفاعل أدناه ، إذا قمنا بإزالة أو إضافة ثاني أكسيد الكربون2 (ز) أو CO(ز)، سيكون هناك تحول في التوازن. ولكن إذا قللنا أو أضفنا C(س)، لن يحدث شيء مع التوازن الكيميائي:
ج(ق) + كو2 (ز) ↔ 2 شركة(ز)
بقلم جينيفر فوغاسا
تخرج في الكيمياء
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/quimica/variacao-concentracao-deslocamento-equilibrio-quimico.htm
