تُعرَّف السعة التي يجب أن تجتذب الشحنات الكهربائية على أنها القدرة على جذب الشحنات الكهربائية ، والتي تأخذ طابعًا مختلفًا اعتمادًا على الاتصال حيث توجد.
فيما يتعلق بالرابط الأيوني والتساهمي ، أيهما سيكون قطبيًا أم غير قطبي؟
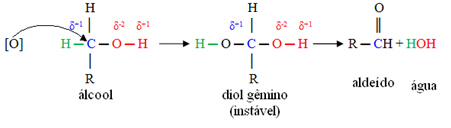
المركبات الأيونية مشحونة بشحنات كهربائية: الكاتيونات والأنيونات ، والتي تسمى الأقطاب الموجبة والسالبة على التوالي. هذه ممثلة بالعلامات δ + و δ-. تتفاعل المواد الأيونية مع المركبات الأخرى بسبب وجود هذه الأقطاب التي تجعل الرابطة غير مستقرة. مثال: تؤدي الرابطة الأيونية بين ذرات الكلور والصوديوم إلى ظهور مركب كلوريد الصوديوم (Na + Cl-) ، المعروف شعبياً باسم ملح الطعام.
باختصار: كل رابطة أيونية هي رابطة قطبية.
يتم تصنيف المركبات التساهمية في الغالب على أنها غير قطبية.
لكن تذكر: هذا لا يعني أن كل مركب تساهمي غير قطبي. ترتبط الأقطاب مع الكهربية ، إذا كانت الرابطة التساهمية بين ذرات من نفس الكهربية ، فإن الرابطة ستكون غير قطبية ، لأنه لا يوجد تكوين للأقطاب.
مثال: المركب التساهمي C3ح8 (البروبان) غير قطبي ، دعنا نرى لماذا:
H H H
│ │ │
ح ج ─ ج ─ ج ─ ح
│ │ │
H H H
لاحظ أن الترابط يحدث بين العناصر المتساوية ، لذلك لديهم نفس مقياس الكهربية.
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
بقلم ليريا ألفيس
تخرج في الكيمياء
فريق مدرسة البرازيل
شاهد المزيد:
لا تنسى الكهرسلبية
اعرف العناصر الأكثر كهرسلبية
كيمياء عامة - كيمياء - مدرسة البرازيل
هل ترغب في الإشارة إلى هذا النص في مدرسة أو عمل أكاديمي؟ نظرة:
سوزا ، ليريا ألفيس دي. "قطبية الروابط الأيونية والتساهمية" ؛ مدرسة البرازيل. متوفر في: https://brasilescola.uol.com.br/quimica/polaridade-das-ligacoes-ionica-covalente.htm. تم الوصول إليه في 27 يونيو 2021.