واحد تفاعل الاستبدال يعتمد على التبادل بين مكونات اثنين من الكواشف المختلفة. من المرجح أن تخضع المركبات ذات الثبات الأكبر (المشبعة ، أي التي تحتوي على روابط بسيطة فقط بين الكربون) لهذه العملية. ومع ذلك ، يمكن للبنزين أيضًا أن يفعل ذلك.
نحن نعلم ذلك في هيكل البنزين هناك ثلاث روابط مزدوجة (ثلاثة روابط pi) ، أي أن هذا المركب غير مشبع ، لكن هذه الأزواج تخضع لظاهرة الرنين (تناوب موضع روابط pi الثلاثة) طوال الوقت. لهذا السبب ، يتمتع هيكلها بقدر أكبر من الاستقرار ، حيث أن الروابط تمر عبر جميع الكربون.
تفاعلات الاستبدال التي يمكن أن تحدث في البنزين هي:
الهلجنة.
نترات.
سلفونة.
ألكلة
أسيلة.
أ) الهلجنة
في هذا التفاعل ، يتفاعل البنزين مع الهالوجينات (Br2، Cl2 مهلا2) ، دائمًا مع وجود محفز ، والذي يمكن أن يكون ملحًا غير عضوي (AlCl3، FeCl3 و FeBr3). تحدث العملية مع تبادل هيدروجين بنزين لذرة هالوجين. والنتيجة هي تشكيل هاليد عضوي وهيدريد المهلجن. شاهد مثالاً:
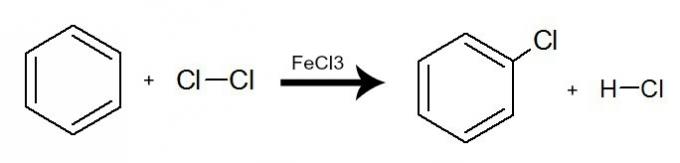
معادلة تمثل الهالوجين للبنزين باستخدام الكلور الجزيئي (Cl2)
ب) النترات
في هذا التفاعل ، يتفاعل البنزين مع حمض النيتريك (HNO3) ، دائمًا مع وجود محفز حامض الكبريتيك (H
2فقط4) والتدفئة. تحدث العملية مع تبادل الهيدروجين من البنزين لمجموعة NO2 من الحمض. والنتيجة هي تشكيل أ مركب نيترو و الماء.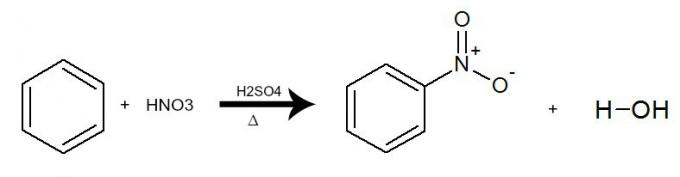
معادلة تمثل نترات البنزين باستخدام حمض النيتريك
ج) Sulphonation
في هذا التفاعل يتفاعل البنزين مع حامض الكبريتيك (H2فقط4) ، دائمًا مع وجود محفز ثلاثي أكسيد الكبريت (SO3) والتدفئة. تحدث العملية مع تبادل الهيدروجين من البنزين بواسطة مجموعة SO3H من حامض. والنتيجة هي تشكيل حامض سلفونيك و الماء.
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
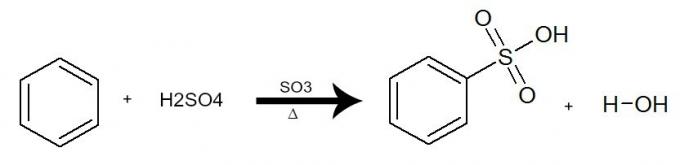
معادلة تمثل سلفونة البنزين باستخدام حامض الكبريتيك
د) الألكلة
في هذا التفاعل ، يتفاعل البنزين مع أ هاليد عضوي (RX)، دائمًا بحضور عامل حفاز ثلاثي كلوريد الألومنيوم (AlCl3) والتدفئة. تحدث العملية بتبادل الهيدروجين من البنزين بواسطة المجموعة R (البديل العضوي) من الهاليد. والنتيجة هي تكوين هيدروكربون عطري متفرعوحمض غير عضوي (HX).
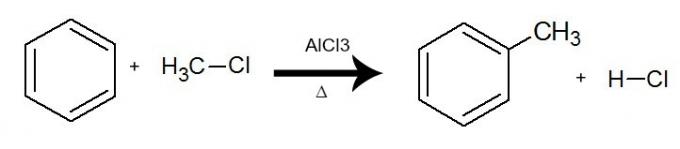
معادلة تمثل ألكلة البنزين باستخدام ميثان الكلور
ه) أسيلة
في هذا التفاعل ، يتفاعل البنزين مع حمض هاليد ، والذي يمكن أن يمثله كلوريد إيثانويل:
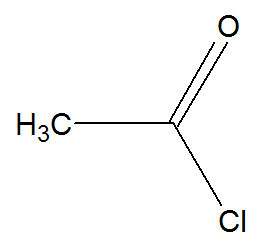
الصيغة الهيكلية لكلوريد الإيثانويل
يحدث رد الفعل مع وجود عامل حفاز ثلاثي كلوريد الألومنيوم (AlCl3) وهناك تبادل واحد من الهيدروجين من البنزين لمجموعة هاليد الحمض بأكملها (باستثناء X- هالوجين). والنتيجة هي تشكيل أ كيتون وحمض غير عضوي (HX). شاهد مثالاً:
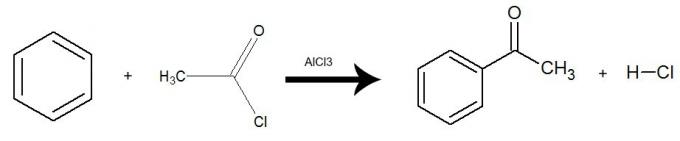
معادلة تمثل أسيلة البنزين باستخدام كلوريد الإيثانويل
بي ديوغو لوبيز دياس
هل ترغب في الإشارة إلى هذا النص في مدرسة أو عمل أكاديمي؟ نظرة:
DAYS ، ديوغو لوبيز. "تفاعلات الاستبدال في البنزين" ؛ مدرسة البرازيل. متوفر في: https://brasilescola.uol.com.br/quimica/reacoes-substituicao-no-benzeno.htm. تم الوصول إليه في 27 يونيو 2021.
كيمياء

المركبات العطرية ، الأرينات ، القطبية ، المذيبات غير القابلة للذوبان ، القابلة للذوبان ، غير القطبية ، الأثير ، رابع كلوريد الكربون ، الهيدروكربونات ، المبيدات الحشرية ، الأصباغ ، المذيبات ، المتفجرات ، المواد المسرطنة ، التولوين ، الميثيل بنزين ، الأدوية ، الصمغ صانع الأحذية.
كيمياء

انقر هنا وتعرف على المزيد حول تفاعل الاستبدال ، وهي عملية كيميائية تقوم فيها الكواشف (العضوية وغير العضوية) بتبادل أحد مكوناتها مع بعضها البعض ، لتشكيل مواد جديدة. من بين المواد الأكثر استخدامًا ككواشف الألكانات والبنزين والهاليدات العضوية.

