في القوى بين الجزيئات هي موضوع في الكيمياء يمكن ، بالتأكيد ، أن يظهر في امتحان المدرسة الثانوية الوطنية (وإما). لذلك ، يجدر التحقق من المحتويات الرئيسية لهذا الموضوع في هذه المقالة.
تعريف
القوى بين الجزيئات إنها قوى - متفاوتة الشدة (ضعيفة أو متوسطة أو قوية) - للتجاذب الكهروستاتيكي أو الروابط القائمة بين جزيئات المادة التي تحافظ على الاتحاد بينهما.
أنواع القوى بين الجزيئات
ال) ثنائي القطب الناجم
و ال قوة الجزيئات التي تحدث بين جزيئات مادة ذات خاصية غير قطبية. يحدث ، على سبيل المثال ، بين جزيئات المواد مثل O2، ح2، لا2، CO2، CH4.
يحدث الاتحاد بين هذه الجزيئات عندما يتم إنشاء ثنائي القطب بينهما. يحدث هذا عندما تقوم الإلكترونات من جزيء بإزاحة الإلكترونات عن آخر ، مما يؤدي إلى إنشاء قطب سالب وموجب ، يتم نقله من جزيء إلى آخر.
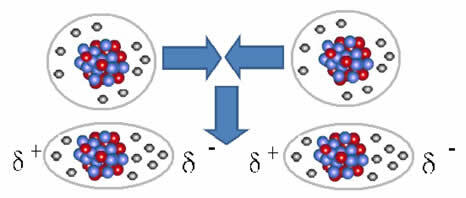
تمثيل تكوين ثنائي القطب في الجزيئات غير القطبية
بين هذه الجزيئات ، تم تشكيل قطبين ، ويتفاعل القطب السالب لأحدهما مع القطب الموجب للآخر. لأن هذه الأقطاب تم إنشاؤها ، فهي قوة بين جزيئات منخفضة الكثافة.
ب) دائم ثنائي القطب
و ال قوة الجزيئات التي تحدث بين جزيئات مادة ذات خاصية قطبية. ومن الأمثلة على ذلك جزيئات مواد مثل HCN و H2أوه ، نيو هامبشاير3، أول أكسيد الكربون ، CH3Cl.
يحدث الاتحاد بين هذه الجزيئات عندما يتفاعل القطب السالب لأحدهما مع القطب الموجب للآخر.
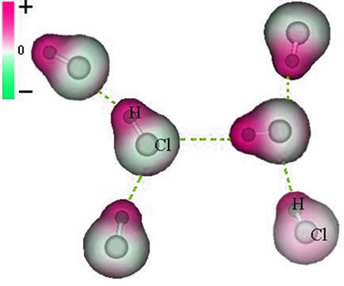
تمثيل القوة ثنائية القطب الدائمة بين جزيئات حمض الهيدروكلوريك
نظرًا لوجود القطبين بالفعل ، فإن القوة بين الجزيئات ثنائية القطب الدائمة تكون أكثر كثافة من ثنائي القطب المستحث.
ç) روابط هيدروجينية
الذي - التي قوة الجزيئات يحدث بين الجزيئات القطبية التي تحتوي على ذرة هيدروجين مرتبطة مباشرة بذرة أكسجين أو نيتروجين أو فلور.
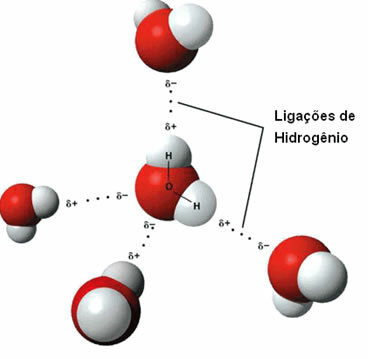
تمثيل روابط الهيدروجين بين جزيئات الماء
تتشكل رابطة الهيدروجين عندما يتفاعل الهيدروجين في جزيء واحد مع الأكسجين أو النيتروجين أو الفلور في الجزيء الآخر.
د) ثنائي القطب أيون
تحدث هذه القوة بين الجزيئات بين الجزيء القطبي ، الذي يحتوي على زوج من الإلكترونات غير المترابطة ، وأيون (كاتيون أو أنيون) في المحلول.
يحتوي جزيء الماء ، على سبيل المثال ، على زوجين من الإلكترونات غير المرتبطة في الأكسجين. إذا كانت هناك أيونات في الوسط المائي ، فإنها تقترب من جزيء الماء ، حيث توجد أقطاب فيه.
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
أهمية
أهمية معرفة القوى الجزيئية للعدو إنه الفهم الذي يجلبونه فيما يتعلق بالحالات الفيزيائية ونقطة الانصهار ونقطة الغليان وقابلية المواد للذوبان.
ال) العلاقة مع نقطة انصهار وغليان المادة
تشير نقطة الانصهار إلى درجة حرارة الانتقال من الحالة الصلبة إلى الحالة السائلة ، وتشير نقطة الغليان إلى درجة حرارة الانتقال من الحالة السائلة إلى الحالة الغازية.
يرتبط هذا المقطع ارتباطًا مباشرًا بالتفاعل بين جزيئات المادة ، لأن ما يميز حالة فيزيائية عن أخرى هو مستوى التجمع بين جزيئاتها.
وبالتالي ، كلما زادت كثافة القوة بين الجزيئات ، زادت نقاط الانصهار والغليان. كلما قلت شدة القوة بين الجزيئات ، قلت نقاط الانصهار والغليان. وبالتالي ، يمكننا تحديد الترتيب التنازلي لنقطة الانصهار والغليان:
الرابطة الهيدروجينية> ثنائي القطب الدائم> ثنائي القطب المستحث
ب) علاقة الذوبان
بشكل عام ، يجب أن نعرف أن مثل يذوب مثل ، أي مادة قطبية تذوب المادة القطبية والمادة غير القطبية تذوب مادة غير قطبية.
ومع ذلك ، لا تزال هناك إمكانية للتفاعل بين الجزيئات الذائبة وجزيئات المذيب. يحدث هذا فقط إذا كان هذا التفاعل الجديد أكبر مما هو موجود بالفعل بين جزيئات المادة نفسها.
مثال على تطبيق القوة بين الجزيئات في Enem
المثال الأول: (Enem-2011) يكتسب جلد الإنسان ، عندما يكون رطبًا جيدًا ، مرونة جيدة ومظهرًا ناعمًا وسلسًا. من ناحية أخرى ، عندما يجف ، يفقد مرونته ويظهر معتمًا وخشنًا. لمنع جفاف الجلد ، من الضروري ، كلما أمكن ، استخدام مرطبات ترطيب ، مصنوعة بشكل عام من الجلسرين والبولي إيثيلين جلايكول:

إن احتباس الماء على سطح الجلد الذي تعززه المرطبات هو نتيجة تفاعل مجموعات الهيدروكسيل لعوامل الترطيب مع الرطوبة الموجودة في البيئة من خلال:
أ) الروابط الأيونية
ب) قوات لندن
ج) الروابط التساهمية
د) قوى ثنائي القطب ثنائي القطب
هـ) روابط الهيدروجين
الإجابة على هذا السؤال هي الترابط الهيدروجيني ، لأن جزيء الماء يرتبط بهيدروجين بذرة أكسجين. يحدث الشيء نفسه مع جزيئات البروبيلين جليكول والبولي إيثيلين جلايكول ، وهي حالة مواتية لحدوث هذا النوع من القوة بين الجزيئات.
بي ديوغو لوبيز دياس
هل ترغب في الإشارة إلى هذا النص في مدرسة أو عمل أكاديمي؟ نظرة:
DAYS ، ديوغو لوبيز. "القوى الجزيئية في العدو" ؛ مدرسة البرازيل. متوفر في: https://brasilescola.uol.com.br/quimica/forca-intermoleculares-no-enem.htm. تم الوصول إليه في 27 يونيو 2021.