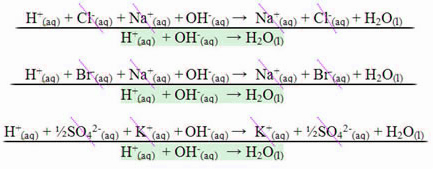ال سلسلة تماثل هو نوع من التماثل المسطح أو الدستوري ، أي حيث يكون لمركبين أو أكثر نفس الشيء الصيغة الجزيئية (نفس العناصر الكيميائية وبنفس المقدار) لكنها تختلف حسب الصيغة الهيكلي.
في حالة التماثل المتسلسل (يُطلق عليه أيضًا اسم التزاوج الأساسي أو التماثل الهيكلي) ، تنتمي المركبات إلى نفس الوظيفة العضوية ، ولكن الاختلاف في نوع السلسلة.
على سبيل المثال ، يمكن أن يكون لدينا الحالات التالية:
1 - يمكن أن يكون لأحد الأيزومر سلسلة مفتوحة (لا دورية) ، بينما يحتوي الآخر على سلسلة مغلقة (دورية) ؛
2 - يمكن أن يحتوي أيزومر واحد على سلسلة مشبعة (روابط مفردة فقط بين الكربون) ، بينما الأيزومر الآخر غير مشبع (له رابطة مزدوجة واحدة على الأقل بين الكربون) ؛
3 - أحدهما لديه سلسلة عادية ، والآخر لديه سلسلة متفرعة ؛
4 - أحدهما لديه سلسلة متجانسة ، والآخر لديه سلسلة غير متجانسة.
إذا كان لديك أي أسئلة حول هذه الأنواع من سلاسل الكربون ، فاقرأ النص تصنيف سلاسل الكربون.
انظر الآن إلى بعض الأمثلة على التماثل المتسلسل:
1- السلسلة المفتوحة والمغلقة:
الأيزومرات التالية لها الصيغة الجزيئية C5ح10، لكنهما يختلفان في حقيقة أن أحدهما لديه سلسلة مفتوحة والآخر به سلسلة مغلقة:

ايزومرات سلسلة (مفتوحة ومغلقة)
بالإضافة إلى ذلك ، يتناسب هذا المثال أيضًا مع النوع التالي من التماثل المتسلسل:
2- السلسلة المشبعة وغير المشبعة:
في المثال السابق ، رأينا أن سلسلة pent-1-ene غير مشبعة ، حيث تحتوي على رابطة مزدوجة بين كربونين ، في حين أن السيكلوبنتان مشبع ، أي أنه يحتوي فقط على روابط مفردة.
شاهد مثالاً آخر: الصيغة الجزيئية: C3ح6:
CH2 CH ─ CH3 و CH2
/ \
ح2C CH2
البروبين سيكلوبروبان
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
3- سلسلة عادية ومتفرعة:
يمكن أن يحدث هذا النوع من التماثل في سلاسل مغلقة أو مفتوحة. على سبيل المثال ، فإن السيكلوبنتان الموضح في العنصر الأول ليس له فروع ، ولكن هناك أيزومرات أخرى لها ، وهي ميثيل سيكلوبوتان ، تعمل. نظرة:

ايزومرات سلسلة (عادية ومتفرعة)
انظر الآن إلى مثال على هذا النوع من تماثل السلسلة المفتوحة. الصيغة الجزيئية للأيزومرات التالية هي: C4ح8ا2:
ح3C CH2 CH2─ COOH و CH3 ─ CH ─ COOH
│
CH3
حمض البوتانويك 2-ميثيل بروبانويك أسيد
4- سلسلة متجانسة وغير متجانسة:
السلسلة المتجانسة هي تلك التي تحتوي على ذرات كربون فقط ، بينما السلسلة غير المتجانسة هي تلك التي تحتوي على ذرة غير متجانسة ، أي ذرة بعض العناصر الكيميائية بين الكربون ، مثل الأكسجين والنيتروجين والكبريت و الفوسفور.
مثال: ج2ح7ن:
ح3ج ─ ن CH3 و ح3C CH2 ─ نيو هامبشاير2
│
ح
ثنائي ميثيلامين إيثيل أمين
(غير متجانس) (متجانس)
بقلم جينيفر فوغاسا
تخرج في الكيمياء
هل ترغب في الإشارة إلى هذا النص في مدرسة أو عمل أكاديمي؟ نظرة:
فوغا ، جينيفر روشا فارغاس. "سلسلة الايزومرية" ؛ مدرسة البرازيل. متوفر في: https://brasilescola.uol.com.br/quimica/isomeria-cadeia.htm. تم الوصول إليه في 27 يونيو 2021.
كيمياء
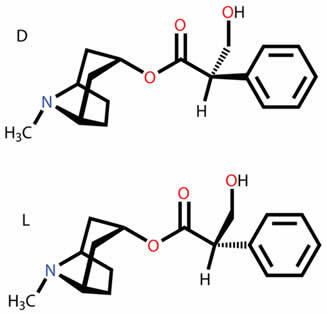
تعرف على الأنواع المختلفة من الأيزومرات المستوية والمكانية ، مثل الوظيفة ، والموضع ، والسلسلة ، والتوتومرية ، والميتامرية ، والتماكب الهندسي العابر والمتماثل البصري.