У валентній оболонці вуглець має чотири електрони, а це означає, що він може утворювати чотири зв’язки, отже, він може приєднуватися до інших атомів. як: H, O, N, Cl. Ця властивість вуглецю пояснює різноманітність органічних сполук, що існують у природі, саме тому кажуть, що вуглець є чотиривалентний.
У 1874 році Вант Хофф і Ле Бель створили просторову модель вуглецю. Ця модель мала атоми вуглецю, представлені регулярними тетраедрами, причому вуглець займав центр тетраедра, а його чотири валентності відповідали його чотирьом вершинам.
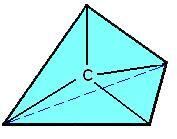
Просторова формула вуглецю.
У цій моделі різні типи зв’язків, що виникають між атомами вуглецю, були представлені наступним чином:
The) просте посилання - тетраедри з’єднані між собою вершиною (одинарний зв’язок);


б) Подвійний зв’язок - тетраедри з'єднані двома вершинами (ребром);

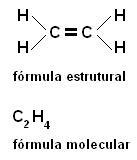
в) Потрійне посилання - тетраедри об’єднані трьома вершинами (одна грань);
Не зупиняйтесь зараз... Після реклами є ще щось;)

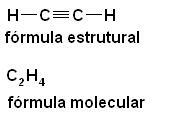
Еволюція атомної моделі показала, що атом має ядро та електросферу, що дозволило появу нових моделей щоб пояснити зв'язки, утворені вуглецем: у 1915 році Льюїс представив нову пропозицію щодо зв'язку атомів вуглець. За словами Льюїса, атоми зв’язані через електронні пари у валентному шарі. Це подання називалось електронною формулою Льюїса, а тип зв’язку, в якому атоми з’єднуються за допомогою електронних пар, відомий як ковалентний зв’язок.

Льюїс Електронна Формула
Переважна більшість органічних молекул є тривимірними, тому виникає необхідність у використанні моделей, які показують не тільки структуру, а й геометрію. Тому просторова формула більше підходить для розуміння структури вуглецю.
Лірія Алвес
Закінчив хімію
Шкільна команда Бразилії
Органічна хімія - Хімія - Бразильська школа
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
СУЗА, Лірія Алвес де. "Структурні формули вуглецю"; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/formulas-estruturais-carbono.htm. Доступ 28 червня 2021 року.