В реакції органічного додавання дуже поширені та вивчені. Варто пам'ятати, що це тип реакції, який представляється основним і переважним механізмом розірвати посилання, або посилання, pi так що два або більше атомів можуть почати бути частиною ланцюга.
Приклад використання реакцій додавання пов'язаний з виробництво маргарину. Цей продукт, настільки поширений у повсякденному житті людей, утворюється в результаті гідрування (реакції приєднання) рослинних олій, які присутні пі посилання у своїй конституції.
Типи реакцій приєднання:
гідрування (додавання атомів водню);
Галогенування (додавання атомів галогену: Cl2, бр2, Я2 та F2);
Реакція з галогенідом (додавання галогенвмісних неорганічних гідрацидів, таких як HCl, HI, Hbr та HF);
Гідратація (додавання гідронію, H+і гідроксил, OH-).
Під час додавання користувачем гідратація або з галогенідом, Правління Марковникова для нас дуже важливо передбачити продукти, які будуть утворюватися. За цим правилом маємо, що атом гідроній (H+) з неорганічного гідроксиду або води
більше гідрованого вуглецю подвійного зв'язку. вже галоген (Cl, Br, I, F) галогеніду або гідроксил (OH-) води буде додано до менше гідрованого вуглецю посилання pi. Див. Приклад застосування цього правила в наступному рівнянні: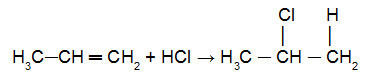
Реакція пропрену з HCl
У цьому рівнянні ми бачимо, що атом (Cl) додавали до менш гідрованого вуглецю посилання pi, тоді як атом гідроній (H+) був доданий до найбільш гідрованого атома вуглецю посилання pi.
є лише одна виняток до правління Марковникова: Реакція Хараша. У ній відбувається інверсія, тобто атом гідроній (H+) буде додано до менше гідрованого вуглецю дає посилання pi, це галоген (Br) галогеніду буде додано до більше гідрованого вуглецю дає посилання pi. Деталь у тому, що ця реакція відбувається лише одним способом:
Не зупиняйтесь зараз... Після реклами є ще щось;)
Наявність органічної перекису;
Використання Hbr.
ПРИМІТКА: якщо ці умови не виконуються, Правління Марковникова буде використовуватися нормально.
Дивіться нижче заявку на Реакція Хараша в пропілені:
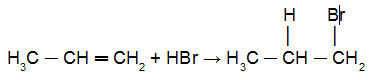
Реакція пропену з HBr у присутності перекису
ПРИМІТКА: Варто зазначити, що органічна пероксид - це сполука, яка обов’язково має групу (R─O─O─R) у своєму складі. Найбільш використовувана органічна пероксид в реакціях Хараша отримується з карбонових кислот і має таку структуру:
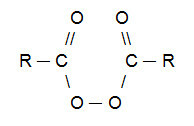
Загальна структурна формула органічної пероксиду
Пояснення реакції Хараша на перетворення правила Марковникова полягає в тому, що спочатку перекис розщеплюється (крок 1), утворюючи вільні радикали з двома атомами кисню, які атакують водень HBr (крок 2). З цієї причини, хто спочатку атакує молекулу алкену, буде Br (крок 3). Тільки після того, як водень зв’яжеться з алкенним ланцюгом. Дотримуйтесь послідовності фактів:
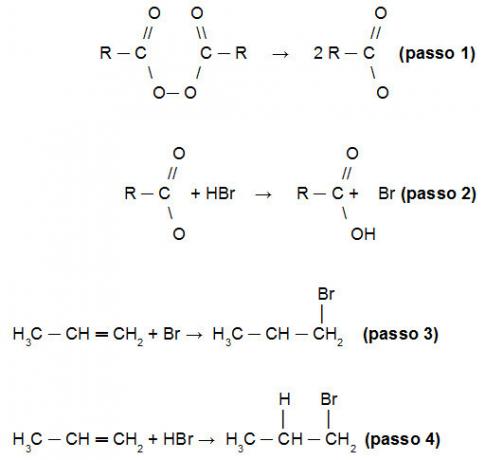
Демонстрація механізму реакції Хараша
Мені Діого Лопес Діас
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
ДНІ, Діоґо Лопес. «Реакція Хараша»; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/reacao-kharash.htm. Доступ 28 червня 2021 року.



