При вивченні термології ми називаємо це адіабатичні перетворення ті газоподібні перетворення, де відсутній теплообмін із зовнішнім середовищем. Отже, при адіабатичному перетворенні теплота дорівнює нулю.
Q = 0
Якщо ми застосовуємо Перший закон термодинаміки, то маємо:
Q = ∆U + τ
∆U = - τ
Але що це означає, що між зовнішнім середовищем немає теплообміну? Це означає, що якщо відбувається газоподібне розширення і газ виконує роботу 300 Дж, це не відбувається якщо відбувається теплообмін із середовищем, коливання внутрішньої енергії газу буде негативним, отже, ми матимемо:
∆U = - 300 Дж
Тепер, якщо спостерігається зменшення внутрішньої енергії газу, можна сказати, що відбулося також зниження температури газу. Із загального закону газів

можна сказати, що якщо об’єм збільшується, а температура газу знижується, обов’язково зменшиться і тиск газу. Взагалі кажучи, можна сказати, що те саме відбувається і при стисненні, тому що якщо відбувається стиснення, внутрішня енергія газу збільшиться, отже і тиск також зросте.
Карта розуму: Адіабатична трансформація
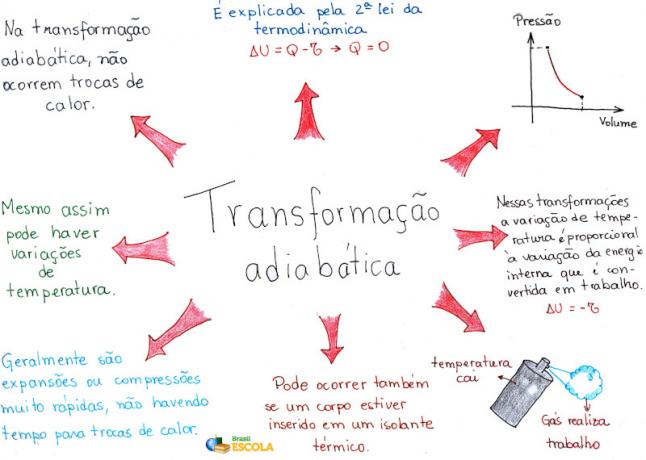
* Щоб завантажити карту розуму в PDF, Натисніть тут!
Коротко можна сказати, що:
- при адіабатичному розширенні температура і тиск знижуються;
- при адіабатичному стисненні підвищуються як температура, так і тиск.
Таблиця нижче дає огляд адіабатичного перетворення:
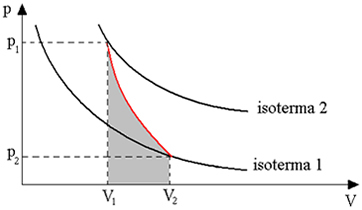
Адіабатичні перетворення отримують за допомогою теплоізольованих контейнерів, а також шляхом стиснення або дуже швидкого розширення.
Таким чином, ми можемо зробити висновок, що коли газ обмінюється теплом із зовнішнім середовищем, потрібен певний час, щоб тепло поширилося через газоподібну масу і прийшло в рівновагу. Отже, коли здійснюється як розширення, так і швидке стиснення, теплообмін із зовнішнім середовищем практично відсутній.
* Карта розуму від мене Рафаель Хелерброк
Доміціано Маркес
Закінчив фізику
Джерело: Бразильська школа - https://brasilescola.uol.com.br/fisica/estudo-transformacao-adiabatica.htm
