Газідеально це той, де зіткнення між частинками ідеально еластичні. Між його частинками немає ніякої взаємодії, наприклад сили привабливі або відразливі, до того ж ці частинки не займають місця.
Відповідно з кінетична теорія газів, термодинамічний стан ідеального газу повністю описується змінними тиску, обсяг і температури.
Дивисьтакож: Калориметрія: карта розуму, формули та розв’язані вправи
концепція ідеального газу
Ідеальні гази складаються виключно з частинкиврозмірипунктуальний (незначного розміру), які знаходяться в руххаотичний увімкнено високийшвидкість. У цьому типі газу температура і швидкість перекладу частинок пропорційні.
Оскільки між частинками ідеального газу немає взаємодії, то внутрішня енергія цього газу завжди дорівнює сумі кінетична енергія всіх частинок, що його складають.
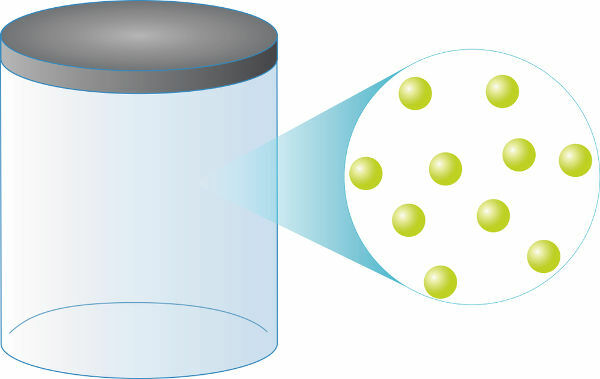
Якими б не були ідеальні гази, вони завжди матимуть однакові номервчастинки для того ж обсягу. Їх маса, в свою чергу, буде залежати безпосередньо від вашого
молярна маса (вимірюється в г / моль), крім того, 1 моль ідеального газу (приблизно 6.0.1023 частинки) завжди будуть займати a об’єм, що дорівнює 22,4 л.ти газисправжній, де є поява зіткненнянееластичний між частинками дуже наближаються до поведінки ідеальних газів у режими низького тиску та високих температур. За збігом обставин, за нормальних умов тиску і температури на Землі (25 ° С і 1 атм) більша частина гази поводяться як ідеальні гази, і це полегшує обчислення прогнозів щодо термодинамічної поведінки їх.
Деякі гази, наприклад водяна пара, який розбавляється в атмосферний газ, не можна вважати ідеальними газами, але так газисправжній. Ці гази мають значну взаємодію між їх частинками, що може конденсувати, викликаючи їх зріджувати, якщо він є перепад температури.
Характеристика ідеальних газів
Перевірте це на реферат, деякі характеристики ідеальних газів:
- У них відбуваються лише ідеально пружні зіткнення між частинками;
- У них відсутні взаємодії між частинками;
- У них частинки мають незначні розміри;
- 1 моль ідеального газу займає об’єм 22,4 л, незалежно від того, що це за газ;
- Реальні гази поводяться як ідеальні гази, коли перебувають під режимами низького тиску та високих температур;
- Більшість газів поводяться подібно до ідеальних газів.
закон ідеального газу
Вивчення газів розроблено вченими Чарльзбойл,ЙосипЛуїгей-люссак і Робертбойл призвело до появи Росії три емпіричні закони, що використовується для пояснення поведінки ідеальних газів в режимах температури, тиску і гучністьконстанти, відповідно.
Разом ці закони склали необхідну основу для виникнення Росії закон ідеального газу, що стосується початковий термодинамічний стан газу, що визначається величинами P1, Т1 і V1, З твоїм кінцевий термодинамічний стан (Стор2, V2 і Т2), переживши деякі перетворення газу.
Перевірте формула загального газового закону:
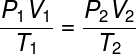
Загальний газовий закон стверджує, що продукту дає тиску хутро гучністьзгаз, розділене на термодинамічну температуру, в кельвінах, дорівнює константі. Ця константа, в свою чергу, описується клапейронне рівняння, дивіться:
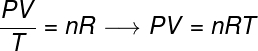
немає - кількість родимок (моль)
Р. - універсальна константа ідеальних газів (0,082 атм. Л / моль. К або 8,31 Дж / моль. К)
У формулі P - тиск, який чинить газ, V - обсяг, який займає цей газ, і Т - температура, виміряна в кельвінах. велич немає відноситься до кількості родимок, тоді як Р. є універсальною константою ідеальних газів, яка часто вимірюється в одиницях атм. л / моль. К або в Дж / моль. K, остання прийнята SI.
Дивисьтакож:Що таке сонячний вітер і як він впливає на атмосферу Землі?
Внутрішня енергія ідеального газу
THE енергіявнутрішній ідеальних газів можна розрахувати за допомогою добутку між постійнийвБольцмана і термодинамічної температури, зверніть увагу:
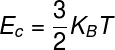
КB - постійна Больцмана (КB = 1,38.10-23 J / K)
З попереднього співвідношення, яке дозволяє нам розрахувати середня кінетична енергія з частинок ідеального газу виводимо наступну формулу, за якою можна розрахувати, що таке середня квадратична швидкість молекул ідеального газу, для даної температури T, зверніть увагу:
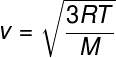
М - молярна маса (г / моль)
Ця формула дозволяє побачити, що a доповненнявтемператури ідеального газу призводить до збільшення середньої квадратної швидкості частинок.
Дізнайтеся більше:З’ясуйте, з чого складається світло і які його характеристики
Розв’язані вправи на ідеальні гази
Питання 1) Два моли ідеального газу при тиску 1 атм знаходяться при температурі 227 ° С. Обчисліть, у літрах, об’єм, який займає цей газ.
Дані: R = 0,082 атм. Л / моль. К
а) 75 л
б) 82 л
в) 15 л
г) 27 л
д) 25 л
Шаблон: Літера Б
Дозвіл:
Для розрахунку об'єму цього газу ми будемо використовувати рівняння Клапейрона, однак перед тим, як зробити розрахунок, необхідно перетворити температуру 227 ° С у кельвін. Для цього ми додаємо коефіцієнт 273 до цієї температури, в результаті чого температура становить 500 К.
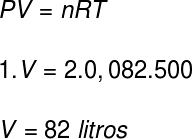
Згідно з резолюцією, об'єм, який займає газ, становить 82 літри.
Питання 2) Ідеальний газ займає об’єм 20 л, коли на нього діє тиск 3 атм, завдяки чому його температура залишається постійною, а об’єм втричі. Обчисліть кінцевий тиск цього газу після того, як він пройшов це перетворення.
а) 1 атм
б) 3 атм
в) 5 атм
г) 8 атм
д) 9 атм
Шаблон: Літера а
Дозвіл:
Для вирішення цієї вправи ми використаємо загальний закон газів, зверніть увагу:
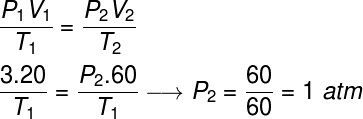
Для розрахунку потрібно було призначити газу об'єм 60 л, оскільки його об'єм потроївся за час перетворення.
Автор: Рафаель Хеллерброк
Вчитель фізики
