активні ізомери або оптично активні ізомери (IOA) - це молекули певної хімічної речовини, які можуть здійснювати поляризацію та відхилення план світло праворуч або ліворуч. Щоб перевірити, чи має речовина активні ізомери, просто перевірте, чи є в її структурній формулі асиметричний вуглець:

Аналізуючи ланцюжок, представлений на зображенні вище, ми можемо побачити, що центральний вуглець має чотири різні ліганди (ОН, Н, СН3 і Cl), що робить його a вуглець асиметричний, який також називають вуглецем хіральний. Таким чином, коли ланцюг має один або кілька хіральних вуглеводнів, будуть активні ізомери.
ти типи активних ізомерів(IOA) вони є:
Правша: Активний оптичний ізомер, який вигинає поляризоване світло вправо;
Левогіро: Активний оптичний ізомер, який вигинає поляризоване світло вліво.
Спостереження: Наявність асиметричного вуглецю в структурній формулі вказує на те, що речовина повинна мати левообертаючий ізомер і правообертаючий ізомер. Ми не можемо знати, в який бік відхилялося світло, оскільки наявність хірального вуглецю вже свідчить про цей факт. Завжди половина існуючих молекул є лівшами, а інша половина - правшами.
Молекули лівої та правої руки будь-якої органічної речовини завжди мають однакові фізичні властивості (точка плавлення, температура кипіння, щільність, розчинність тощо), але присутня хімічна активність (поведінка в організмі) багато різних. Прикладом може служити адреналін. Тільки молекула левогіри адреналіну діє в організмі, тоді як декстрогіра не діє.
Дивіться тепер структурну формулу речовини бутан-2-ол, щоб перевірити, чи має вона активні ізомери чи ні:
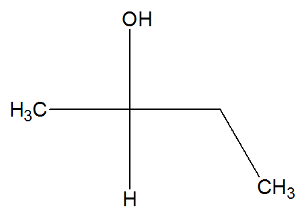
У структурі бутан-2-олу ми можемо спостерігати, що має вуглець 2 чотири різних в'яжучих речовини (ОН, Н, СН3, СН2-CH3), отже це хіральний вуглець і представлений правообертаючим активним ізомером та іншим леворотаторним активним ізомером.
Розрахунок активних ізомерів (IOA)
Голландський хімік Якоб Генрікус Вантно Гофф розробив формулу, яка дозволяє розрахувати, скільки активних ізомерів (IOA) може містити дана речовина. Подивіться:
IOA: 2немає
n: - кількість хіральних вуглеців у структурній формулі речовини.
Дотримуйтесь двох прикладів застосування формули Вантт-Гоффа:
5-дихлор-2,3-дигідрокси-гександіоєва кислота

У структурній формулі сполуки є три хіральні вуглеці або асиметричний, тому:
IOA = 2немає
IOA = 23
IOA = 8
2,3,4,5-тетрагідроксигексанал

У структурній формулі сполуки є чотири хіральні вуглеці (червоні стрілки) або асиметричний, тому:
IOA = 2немає
IOA = 24
IOA = 16
Спостереження: Існує ймовірність того, що структурна формула має два асиметричних вуглецю, які мають абсолютно однакові ліганди. Якщо це відбувається, ми враховуємо в розрахунках лише 1 для значення n, а не 2. Дивіться приклад:
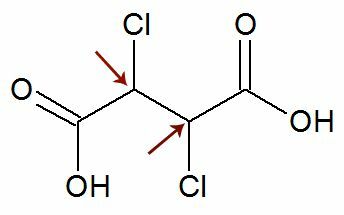
Подібно до два хіральних вуглецю вони є дорівнює, ми розглядаємо лише одне вуглець при розрахунку:
IOA = 2немає
IOA = 21
IOA = 2
Мені Діого Лопес Діас
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/isomeros-ativos.htm
