THE Хімічна кінетика - це область, яка вивчає фактори, що впливають на швидкість розвитку хімічних реакцій, тобто на швидкість, з якою вони відбуваються. У цій галузі проводиться все більше досліджень, оскільки ми часто хочемо пришвидшити одні реакції або сповільнити інші. Це особливо важливо для галузей промисловості, і це дослідження має важливі технологічні наслідки.
Але оскільки швидкість реакції може змінюватися на кожному інтервалі часу і від однієї речовини до іншої, прийнято обчислювати середня швидкість реакції.
Розглянемо наступну загальну реакцію, в якій коефіцієнтами є малі літери, а реактиви та продукти представлені великими літерами:
a A + b B → c C + d D
Буде наведено середню швидкість цієї реакції ділення середньої швидкості реакції будь-якої з реагуючих речовин або середньої швидкості утворення будь-якого з продуктів на відповідний коефіцієнт у хімічному рівнянні. Це дано:
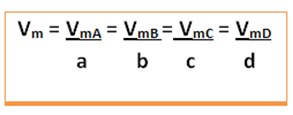
Наприклад, розглянемо реакцію розкладання перекису водню:
2 години2О2 (вод.) → 2 год2О(1) + 1 O2 (г)
Скажімо, за 1 хвилину утворилося 0,3 моль / л Н
2O і 0,15 моль / л O2, тоді як 0,3 моль / л Н розкладається2О2, тобто середні швидкості розкладання та утворення цих речовин у реакції складають:VmH2O2 = 0,3 моль / л. хв
VmH2O = 0,3 моль / л. хв
VmO2 = 0,15 моль / л. хв
Середню швидкість глобальної реакції буде знайдено, взявши одне з цих значень і розділивши його на відповідний коефіцієнт у рівнянні:
Vм = VmH2O2 = 0,3 моль / л. хв = 0,15 моль / л. хв
2 2
Vм = VmH2O = 0,3 моль / л. хв = 0,15 моль / л. хв
2 2
Vм = VmO2 = 0,15 моль / л. хв = 0,15 моль / л. хв
1 1
Зверніть увагу, що три значення рівні, отже, швидкість реакції така ж, як і функція будь-якого реагенту або продукту, за той самий інтервал часу.
Однак як знаходили значення середніх швидкостей кожної з речовин, що беруть участь у цих реакціях?
Це можна розрахувати ділення варіації концентрації речовини (реагенту або продукту) на інтервал часу. Якщо ми збираємося визначити середню швидкість одного з реагенти реакції, нам доведеться поставити a негативний знак до, або ж врахуйте значення концентрації в модулі ||, оскільки, оскільки концентрація реагенту з часом зменшується, значення швидкості буде негативним, але негативної швидкості немає.

Наприклад, розглянемо наступну реакцію розкладання озонового газу (O3 (г)) в кисневому газі (O2 (г)):
2 O3 (г) → 3 O2 (г)
Скажімо, у повітряній кулі було 10 молей газу озону, але через 1 хвилину залишилось лише 4 моля; це означає, що 6 молей озону перетворились на газ кисню. Отже, маємо:
2 O3 (г) → 3 O2 (г)
t = 0 хв 2 моль / л 0 моль / л
сформовані витрати
6 моль / л 9 моль / л
t = 1 хв 4 моль / л 9 моль / л
Зауважте, що оскільки співвідношення реакцій дорівнює 2: 3, то якщо було використано 6 молей O3, Утворилося 9 моль O2. Отже, через 1 хвилину ми маємо такі середні швидкості:
Vм = - ∆ [3]
т
Vм = - ([O3фінал - О3початковий])
тОстаточний - тпочатковий
Vм = - ([4 - 10])
1– 0
Vм = 6 моль / л. хв→ Протягом 1 хвилини 6 моль озону реагували в кожному літрі системи.
Vм = ∆ [2]
т
Vм = ([O2фінал - О2початковий])
тОстаточний - тпочатковий
Vм = ([9 - 0])
1– 0
Vм = 9 моль / л. хв→ Протягом 1 хвилини в кожному літрі системи утворювалося 9 молей кисню.
Це показує нам, що ми можемо розрахувати середню швидкість як функцію реагентів або як функцію продуктів.
Тепер, якщо ми хочемо розрахувати середню швидкість цієї глобальної реакції, просто зробіть те, що ми показали на початку: розділіть кожну з цих швидкостей на відповідні коефіцієнти в хімічному рівнянні:
Vм = VmO3 = 6 моль / л. хв = 3 моль / л. хв
2 21
Vм = VmO2 = 9 моль / л. хв = 3 моль / л. хв
3 3
Vм = VmO3 = VmO2
23
Дженніфер Фогача
Закінчив хімію
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/velocidade-das-reacoes-quimicas.htm
