Гібридизація - це назва, що дається злиттю або об'єднанню неповних атомних орбіталей, явищу, яке збільшує кількість ковалентні зв’язки що може зробити атом. Пам'ятаючи, що орбіталь - це область атома, де є більша ймовірність знайти електрон.
Знати кількість зв’язків, які утворює атом, і зрозуміти явище гібридизація, необхідно знати деякі основні моменти щодо атома:
1О точка: енергетичні підрівні
Енергетичні підрівні, які може мати атом, - це s, p, d, f.
2О точка: кількість орбіталей на підрівень
Кожен підрівня енергії має різну кількість орбіталей, як ми можемо бачити нижче:
Підрівень s: 1 орбітальний;
p підрівень: 3 орбіталі;
Підрівень d: 5 орбіталей.
Загальне представлення цих орбіталей здійснюється наступним чином:
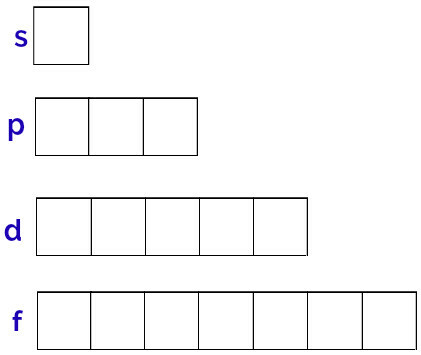
Представлення орбіталей кожного підрівню
На думку Паулі, орбіталя може мати максимум 2 електрони, с обертається (обертальні рухи) навпроти.
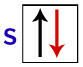
Представлення s-орбіталі з її електронами
За словами Хунда, орбітала підрівню отримує свій другий електрон лише тоді, коли всі інші орбіталі цього підрівню вже отримали перший електрон.
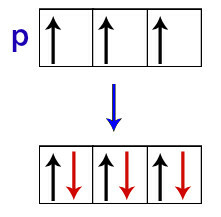
Розподіл електронів на p підрівневих орбіталях
3О пункт: електронний розподіл
Щоб зрозуміти гібридизацію та кількість зв'язків, які утворює атом, важливо здійснити електронний розподіл на діаграмі Лінуса Полінга.

Діаграма Лінуса Полінга
Пам'ятаючи, що максимальна кількість електронів на кожному підрівні:
s = 2 електрони;
p = 6 електронів;
d = 10 електронів;
f = 14 електронів.
Після цього короткого огляду ми можемо визначитись зараз що таке гібридизація. Для цього ми будемо використовувати хімічний елемент бор (атомний номер = 5) як приклад.
Під час електронного розподілу бору ми маємо:
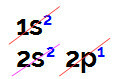
Електронний розподіл бору на діаграмі Лінуса Полінга
У цьому розподілі можна спостерігати, що бор має 2 електрони в s-підрівні та 1 електрон у p-рівні валентний шар.
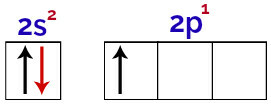
Електрони на орбіталях валентного шару бору
Оскільки бор має 1 неповну орбіталь, тому він повинен утворювати лише один ковалентний зв’язок, оскільки кількість зв’язків завжди безпосередньо пов’язана з кількістю неповних орбіталей.
Таким чином, коли атом бору отримує енергію із зовнішнього середовища, його електрони, особливо ті, що знаходяться у валентній оболонці, збуджуються. Це призводить до того, що один з електронів з s-орбіталі виходить і займає одну з порожніх p-орбіталей, що призводить до 3 неповних атомних орбіталей, як ви можете бачити на наступному зображенні:

Уявлення збудженого стану атома бору
Нарешті, існує об’єднання неповної орбіталі з неповною р-орбіталі. Цей союз називається гібридизація. Оскільки ми маємо злиття s-орбіталі з двома p, це називається гібридизація sp2.
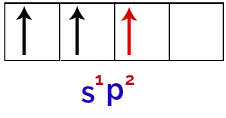
Представлення гібридизованих орбіталей в атомі бору
Крім бору, кілька інших хімічних елементів зазнають явища гібридизації, такі як сірка (S), ксенон (Xe), люмінофор (P), вуглець (Ç), берилій (Будь).
Мені Діого Лопес Діас
Джерело: Бразильська школа - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-hibridizacao.htm
