хімічний елемент фосфор (P) належить до третього періоду Періодичної системи та до сімейства Азоту (VA). З цієї причини його атоми зазвичай складають три хімічні зв’язки щоб досягти теорія октету (стабільність). Однак існують деякі ситуації, коли атом фосфору утворює більше трьох зв’язків, що можливо лише завдяки явище гібридизації.
Щоб зрозуміти гібридизація фосфору, ми повинні спочатку зрозуміти, чому атом цього елемента утворює три зв’язки. Для цього нам просто потрібно контролювати ваш електронний розподіл:

Електронне розподіл фосфору
Ми можемо помітити, що у валентному шарі атом фосфору має повний 3-рівний підрівень (з два електрони) і неповний 3p підрівень (кожна з трьох p підрівнів має орбіталі електрон). Нижче ми маємо розподіл електронів на орбіталях підрівнів Фоленний валентний шар:
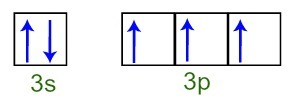
Представлення електронів валентної оболонки атома фосфору
Оскільки кожна з 3р орбіталей підрівню неповна, атом фосфору здатний утворювати три хімічні зв’язки, досягаючи тим самим стабільності.
Тепер, коли ми розглянемо речовину PCl
5, наприклад, ми впевнені, що в цій молекулі фосфор зазнав гібридизації, оскільки він створив п’ять зв’язків. Оскільки хлор, який належить до сімейства VIIA, потребує зв'язку, щоб бути стабільним, і молекула має п’ять атомів цього елемента, кожен з них повинен створити зв'язок, що робить атом фосфору, в свою чергу, також повинен складати п'ять Зв'язки. Це можливе лише через гібридизація (об’єднання неповних атомних орбіталей) фосфору.Отримуючи енергію із зовнішнього середовища, електрони атома Фосфору збуджуються. Незабаром один з двох електронів, що належать до підрівню 3, рухається до порожньої орбіталі, що знаходиться в підрівні d, яка до того часу не має електронів. Див. Схему нижче:
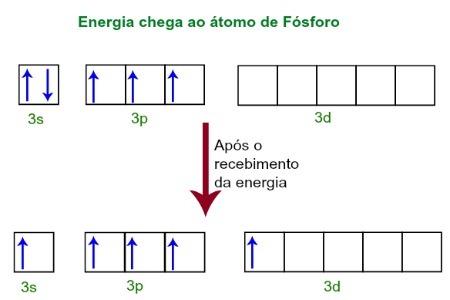
Отримавши енергію, електрони люмінофора збуджуються, і один займає орбіталь d рівня.
На даний момент ми маємо у валентному шарі Фосфору s-орбіталь, три p-орбіталі та неповну d-орбіталь.Зрештою, ці п’ять орбіталей гібридизуються, тобто зливаються, в результаті чого з’являються п’ять неповних атомних орбіталей, які тепер здатні утворювати п’ять хімічних зв’язків.

Гібридизація неповних атомних орбіталей фосфору
Як орбіталя s, три р орбіталі та d орбіталі, гібридизація фосфору має тип sp3d.
Мені Діого Лопес Діас
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/hibridizacao-fosforo.htm