Кислотні оксиди - це ті оксиди, які при взаємодії з водою утворюють кислоту як продукт. При взаємодії з основою продуктами будуть сіль і вода.
Ці сполуки зазвичай мають ковалентний характер, тобто вони є молекулярними, розчиняються у воді і утворюються здебільшого неметалами, які є елементами з високою електронегативністю. Утворені металами, вони мають високі окислювальні числа (електричний заряд).
Приклади:
CO2, ТІЛЬКИ2, ТІЛЬКИ3, С2О5, Кл2О6, БІЛЯ2, немає2О4, немає2О5тощо
Далі наведено загальну схему характерних реакцій для оксидів кислот та приклад:
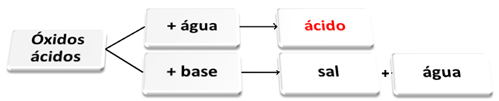
Кислотні оксиди, що реагують з водою та з основою
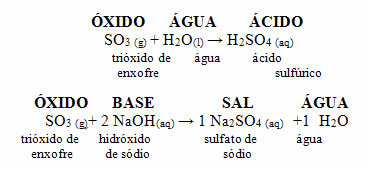
Кислотні оксиди також називають ангідриди, оскільки це слово походить від грецької ангідрос, що означає "немає води", а оксиди кислот можна вважати «безводною кислотою».
Властивості та застосування деяких кислотних оксидів:
• Вуглекислий газ (вуглекислий газ) - CO2:
Ця сполука використовується як газ у безалкогольних напоях та мінеральних водах, оскільки під впливом високого тиску вона розчиняється у воді. У цих продуктах утворюється кисле середовище, оскільки це кислий оксид, який реагує з водою, утворюючи кислоту, відповідно до реакції нижче:

Нижче 78 ° C він знаходиться у твердому стані і відомий як сухий лід, який отримав свою назву, оскільки своїм зовнішнім виглядом нагадує лід. загальний, але він не плавиться, переходячи до рідкого стану при кімнатній температурі, а переходить до стану пари, тобто він сублімує. Таким чином, ця особливість використовується як мальовничий ресурс для концертів, кіно, театрів, вечірок тощо.

Вуглекислий газ - це кислий оксид
Він також виявляється в атмосфері в результаті дихання людини, спалення викопного палива (вугілля, нафтопродуктів, алкоголю тощо) та лісових пожеж. Таким чином, він є одним із відповідальних за кислотні дощі.
• Оксиди сірки - SO2 і ТАК3
Ці оксиди також присутні в атмосфері, маючи природне та штучне походження. Природне відбувається через виверження вулканів та розкладання рослин і тварин. Штучне відповідає найбільшій кількості цих оксидів в атмосфері, як вони є виганяється спалюванням викопного палива, головним чином дизельного масла, яке містить сірку, таку як домішка.
Двоокис сірки (SO2) реагує з киснем з атмосфери, утворюючи триоксид сірки (SO3). Коли цей останній оксид реагує з дощовою водою, утворюється сірчана кислота, яка є дуже сильною і завдає шкоди.
• Спалювання сірки від палива: S + O2 → ОС2
• Перетворення SO2 в SO3: SO2 + ½2 → ОС3
Реакції SO2 і SO3 з водою, що дає кислоти: SO2 + H2O → H2ТІЛЬКИ3
ТІЛЬКИ3 + H2O → H2ТІЛЬКИ4
• тетроксиди азоту (азотно-азотний ангідрид) - N2О4
Ця сполука має температуру кипіння 22ºC, має жовтий колір і досить летюча. Він утворюється в атмосфері окисленням азоту і може бути у рідкій формі, у вигляді димера монооксиду азоту або оксиду азоту (NO2). Вище цієї температури він набуває форми NO2:
N2О4 ↔ НІ2
Це надзвичайно токсичний газ, і його вдихання смертельне. Він також використовується у складі ракетного палива.
Дженніфер Фогача
Закінчив хімію
