THE хасій, із символом Hs і атомний номер 108, є одним із елементів, відомих як трансактиніди. Як і всі елементи цієї групи, він не зустрічається в природі, будучи синтетичним, крім того, що він радіоактивний і нестабільний. Його синтез приписують німецьким лабораторіям Центру досліджень важких іонів Гельмгольца (GSI), м. Дармстадіуму, Німеччина, і його назва було дано на честь німецької землі Гессен, розташованої в центральному регіоні батьків.
Хасій є найважчим елементом, властивості якого аналізуються за допомогою експериментів, проведених самим GSI. Результати були важливими для підтвердження положення Hs в Періодична таблиця, як сприймалася подібність цього елемента з осмієм і рутенієм, легшими елементами 8 групи.
Читайте також:Борій — синтетичний хімічний елемент, названий на честь Нільса Бора
Резюме Хасій
Це синтетичний хімічний елемент, розташований у групі 8 Періодичної системи.
Він був синтезований Gesellschaft für Schwerionenforschung (GSI) у Дармстадіумі, Німеччина.
Це радіоактивний елемент і нестабільний.
Теоретичні та експериментальні дані підтверджують, що його властивості нагадують найлегші елементи своєї групи.
Як трансактинід, він не може вироблятися у великих масштабах, крім того, що він виробляється зі швидкістю кількох атоми.
Не зупиняйся зараз... Після оголошення буде більше ;)
Властивості хасію
Символ: hs
Атомний номер: 108
Атомна маса: 277 ц.у.
Електронна конфігурація: [Rn] 7 с2 5f14 6d6
Найбільш стабільний ізотоп: 269Hs (14 другий період напіввиведення)
Хімічний ряд: група 8; трансактиніди; надважкі елементи.
Характеристики хасію
Хасій - це а синтетичний елемент і найважчий з групи 8. Вважається а трансактинід, саме тому, що він з’являється в періодичній системі після ряду актинідів. Як і всі трансактиніди, хасій є елементом радіоактивний і нестабільний.
Це означає, що його ізотопи досягають мало часу півжиття (час, необхідний для зменшення маси атома вдвічі). В даний час відомо сім ізотопів хасію, маса яких коливається від 264 до 270 о.о. Серед усіх найстійкішим є ізотоп 269Hs, з періодом напіввиведення 14 секунд.
Хоча короткий період напіврозпаду ускладнює вивчення хімічних властивостей трансактинідів, хасію в цьому відношенні пощастило трохи більше. У червні 2001 року було оголошено, що він став найважчий елемент для аналізу властивостей.
Команді вдалося в місті Дармштадіо, Німеччина, виробити близько шести атомів Hs з періодом напіврозпаду приблизно 10 секунд. Хоча здається мало, цього було достатньо, щоб підтвердити, що оксид гасію HsO4, має сильну схожість з оксидами легших елементів 8 групи RuO4 та OsO4, тобто рутеній це осмій.
Дивіться також: Сіборгій — ще один синтетичний хімічний елемент з радіоактивними властивостями і коротким періодом напіврозпаду
Отримання хасій
Трансактиніди мають спільну складність виробництва. Загалом необхідне найсучасніше обладнання, напр прискорювачі частинок. У них іонні види стикаються з елементами високого атомна маса для утворення надважких елементів (до складу яких входить Hs).
У випадку з хасієм дослідження, які підтвердили його позицію в групі 8 Періодичної системи, включали його виробництво шляхом бомбардування магнієм-26 з кюрієм-248 як мішенню.
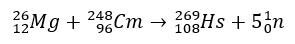
Експерименти за участю цих елементів дорогі, і тому зазвичай проводяться теоретичні дослідження саме для розрахунку та прогнозування хімічних властивостей. Короткий період напіввиведення є ще одним ускладнюючим фактором.
Експериментальні методики поділ і виявлення має бути дуже швидким для отримання достовірних результатів. Нарешті, ефективність реакції цих елементів дуже низька, перебуваючи в діапазоні кількох атомних одиниць.
Запобіжні заходи з Хасієм
Hs не виробляється у великих масштабах, а отже, з ним маніпуляції не передбачає ризиків. Крім того, його отримують у дослідницьких центрах із суворо контрольованим середовищем.
історія Хасію

Трансактиніди були головними героями наукової суперечки через Холодна війна, а Війна трансферів, назва, придумана у зв'язку з суперечками, пов'язаними з виробництвом і розпізнаванням елементів після фермію (Fm, Z = 100). У цьому змаганні брали участь лабораторії:
Об'єднаний інститут ядерних досліджень, м. Дубна, Росія;
Національна лабораторія Лоуренса Берклі в Берклі, Каліфорнія;
Gesellschaft für Schwerionenforschung (GSI, краще перекладається як Центр досліджень важких іонів Гельмгольца) в Дармстадіумі, Німеччина.
У справі з елементом 108 були задіяні групи GSI та Дубна. Однак, хоча дубенські вчені (на чолі з Юрієм Оганесяном) вперше повідомили про наявність елемента 108, представники німецької групи взяли на це заслугу, оскільки GSI показав більш переконливі результати, тоді як в одному експерименті йому вдалося отримати три атоми ізотопу 265, а в іншому — один атом ізотопу 264.
Ці ізотопи були отримані за допомогою універсального лінійного прискорювача (Unilac, краще перекладається як універсальний лінійний прискорювач) з бомбардуванням 208Pb за 58Віра. У 1997 році Міжнародний союз чистої та прикладної хімії (IUPAC) визнав елемент 108 із символом Hs, як Hassium на честь німецької землі Гессен.
Розв’язування вправ на хасій
питання 1
Хасій, символ Hs, вважається найважчим елементом, властивості якого вивчені експериментально. У той час дослідники змогли визначити властивості чотирикису газію, HsO4. У цього виду Hs має такий самий NOx, як і легші елементи його групи, осмій (Os) і рутеній (Ru). Степень окиснення Hs в чотириокисі газію дорівнює:
а) 0
Б) +2
В) +4
Г) +6
E) +8
Роздільна здатність:
Альтернатива Е
THE кисень, коли в а оксид, набуває заряд, рівний -2. Отже, NOx Hs, який ми назвемо x, можна обчислити як:
х + 4(-2) = 0
х - 8 = 0
х = +8
питання 2
Найстабільніший ізотоп хасію Hs має період напіврозпаду всього 14 секунд. Це означає:
А) за 14 секунд маса ізотопу Hs подвоїться.
Б) через 14 секунд маса ізотопу Hs буде меншою за половину початкової маси.
C) трохи менше ніж за хвилину маса ізотопу Hs становитиме 1/16 його початкової маси.
Г) за одну хвилину маса ізотопу Hs становитиме рівно половину його початкової маси.
E) за 14 секунд маса ізотопу Hs поділиться на 4.
Роздільна здатність:
Альтернатива C
Період напіврозпаду вказує час, необхідний для зменшення кількості атомів вдвічі. Це означає, що кожні 14 секунд кількість Hs зменшується вдвічі. Спостерігаючи за цим періодом напіврозпаду, стає ясно, що за 56 секунд вже досягнуто чотири періоди напіврозпаду, внаслідок чого масу Hs ділиться на 24, що становить 16.
Стефано Араухо Новаїс
Вчитель хімії

